傳奇生物下週五於納斯達克上市:母公司持股66%將成受控公司
募資規模爲3.32億至3.69億美元。
據IPO早知道消息,5月29日晚間,傳奇生物向SEC提交的最新招股文件顯示,此次上市將公開發行1842.5萬ADS,同時,母公司金斯瑞(1548.HK)同意以每股首次公開發行價格購買1,200萬美元普通股。發行定價預計在18至20美元/ADS之間。募資規模爲3.32億至3.69億美元。
傳奇生物完成此次IPO後,金斯瑞將持有傳奇生物66%的普通股股份,即66%投票權,意味着傳奇生物將成爲納斯達克交易規則所定義的“受控公司”。
一週前傳奇生物遞交招股書,金斯瑞也發佈了建議分拆傳奇生物納斯達克上市公告。傳奇生物此次上市由摩根士丹利、摩根大通、傑富瑞擔任聯席主承銷商。
傳奇生物是CRO企業金斯瑞旗下自主品牌業務之一,專攻CAR-T細胞免疫療法的跨國子公司。公司爲業界所關注是在2017年美國臨牀腫瘤學會ASCO中,其研發的BCMA雙表位嵌合抗原受體T細胞免疫療法LCAR-B38M在復發/難治性多發性骨髓瘤(R/RMM)患者早期臨牀試驗中表現出了極佳的總緩解率。在當時的黑馬傳奇生物公佈早期數據前,備受關注的CAR-T療法來自於諾華、凱特、巨諾及Bluebird。
5月14日早間,今年第56屆ASCO年會摘要披露了楊森/南京傳奇CAR-T療法最新研究數據:在R/R MM患者的CARTITUDE-1的1b/2期臨牀試驗中,JNJ-4528表現出卓越療效。
金斯瑞曾披露傳奇生物3月9日(美東)向SEC祕密遞表。3月末傳奇生物公佈了其pre-IPO融資,公司獲得了Hudson Bay Capital Management、禮來亞洲基金、VivoCapital、RA Capital Management以及強生旗下的戰略風險投資基金JJDC的1.5億美元投資,投後估值19.5億美元。
2017年12月,傳奇生物與強生旗下楊森達成全球合作和許可協議,雙方共同開發和商業化BCMA CAR-T產品。楊森向金斯瑞支付3.5億美元首期款及後續里程碑付款,創下其時中國藥企對外專利授權首付款最大金額記錄及合作最優條件。
2018年5月,LCAR-B38M獲得美國FDA的IND批件,2019年2月,又獲得美國FDA的孤兒藥資格。2019年4月,LCAR-B38M獲得歐洲藥品管理局(EMA)優先藥物認定(PRIME)資格,是國內首個獲得此認證的CAR-T產品。
據市場調研機構Coherent Market Insights此前的報告,2018年至2028年期間全球CAR-T細胞免疫治療市場的平均年複合增長率將達46.1%,北美和歐洲依舊將佔據大部分市場份額,前者的市場佔有率超過50%。
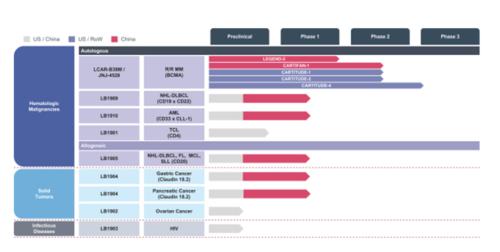
除LCAR-B38M/ JNJ-4528外,傳奇生物其他管線也在進行中,都是處於臨牀早期的自體候選組合,針對各種癌症,包括非霍奇金淋巴瘤NHL、急性髓細胞性白血病AML及T細胞淋巴瘤TCL ,前兩項已在中國啓動了I期臨牀試驗。公司還開發了治療NHL的靶點爲CD20同種異體CAR-T候選藥物,也進入了I期臨牀。另外還有多種針對實體瘤、傳染病的臨牀前和臨牀階段的多種在研產品。
來源:招股書
招股書顯示,公司藥物開發團隊由CEO Yuan Xu博士負責,她曾在默克、吉利德、諾華、安進、凱龍、葛蘭素史克和基因泰克供職,負責藥物研發和商業化。她與傳奇生物其他核心管理人員還將統一參與金斯瑞的管理。傳奇生物上市後金斯瑞股東也將掌握絕大多數股權。
傳奇生物的目標是CAR-T和相關細胞療法在治療血液惡性腫瘤、實體瘤和傳染病方面的研發。在目前商業化較領先的LCAR-B38M / JNJ-4528上,公司計劃通過LCAR-B38M/JNJ-4528的推進,獲得在全球範圍內治療RRMM的批准。據CARTITUDE-1的結果,公司預計於2020年下半年向FDA提交JNJ-4528的適用於R/RMM治療的BLA(生物製品許可申請)。另外,公司還將尋求LCAR-B38M/JNJ-4528在歐洲、中國、日本獲批上市。
目前公司未從產品銷售中獲利。2018、2019年,公司營收分別錄得4913.3萬美元、5726.4萬美元,增幅17%。2018年收入包括楊森的首期款加里程款以及爲金斯瑞提供研發服務所得的100萬美元。2019年的收入的增量幾乎全部來自於里程款的增加。公司同期淨虧損分別爲278.4億美元、1.32億美元。