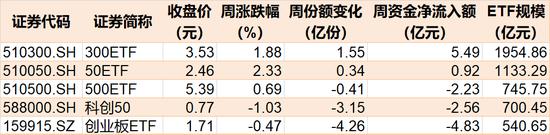
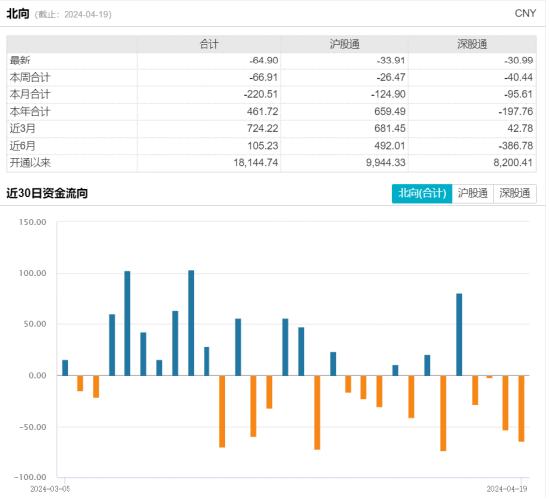
九安醫療有多火?股民緊盯:蹲守觀察、實地調研 甚至有人混進廠區
文 徐玉海、李佳佳
昨日晚間,九安醫療(002432.SZ)發佈補充公告稱美國政府有權隨時因自身因素中止合同。而據財聯社記者瞭解,在這一公告發布前的五小時,即收盤後不久,公司管理層剛剛出面與投資者進行了線上溝通,微信上還出現了“九安機構調研”羣,人數很快到達500位,多名券商醫藥分析師均在其中。

針對備受關注的美國102億元新冠試劑盒訂單情況,九安醫療董事長劉毅在溝通會進一步釋放積極信號。他表示公司正在日夜加班不停趕貨,目前產能規模爲每月2億份,由於原材料配套較爲充分、提產主要靠增加工人,產能仍有提升空間。

劉毅補充稱從公司生產角度來說,公司核心原材料都是外採,因此產能擴張的最大風險也就是僱工。
於具體產能變化和擴產可能性,劉毅笑稱,目前九安醫療工廠門口已經常有蹲守觀察、實地調研的人,甚至發現有人混進其廠區調研的情況。
海外需求居高不下 九安醫療時間窗口優勢明顯
去年12月22日,美國總統拜登宣佈聯邦政府將出資購買5億劑居家新冠檢測試劑,並在2022年1月向美國民衆免費提供。劉毅在電話會上透露,公司本月14日公告的2.5億人份iHealth試劑盒採購訂單即歸屬於美國聯邦政府的此次採購,並要求於兩個月內交齊。
據劉毅介紹,九安醫療持股70%的美國子公司iHealthLabs.Inc一年前開始申請美國FDA EUA授權,當時英國已經開始推行家庭自測的抗原試劑盒,而美國還未真正開始使用。看到這一機會,九安醫療集中調動公司能力進行開發。
作爲並非IVD(體外診斷產品)主力廠家的九安醫療,爲什麼瞄準標準最爲嚴苛的FDA審批?對此劉毅表示,信心主要來自於三點:一是九安醫療以往業務與FDA已有20多年互動,熟悉FDA要求;二是九安做互聯網醫療在美國有七、八十人的團隊,在臨牀、性能、實驗等環節發揮了巨大作用;三是九安美國子公司iHealthLabs.Inc,完全使用自主品牌iHealth,不僅業務毛利率高,也贏得了美國主流市場的認可。
“到目前,實際上美國主流市場上真正能大批量供貨的廠家也很少。”劉毅表示,FDA對抗原試劑盒的審覈非常嚴苛,通過中介機構進行審批申請難以成功。而另一方面,已經通過FDA EUA審批的美國公司,理論上可以在中國尋找代工廠擴大產能規模,但其核心測量的標準等不能隨意改變。
在劉毅看來,居家檢測現在在歐美已經有消費品的屬性。至於家庭檢測能否在更大範圍和國內得以應用,劉毅認爲要取決於疫情控制情況和程度,疫情加重將增加其可能性。
在交流會上,有投資者關心九安醫療後續是否會申請向歐盟等其他國家地區申請使用審批。劉毅對此回應稱暫時不會去,公司要先集中精力做好美國市場,“打好這一仗”。
而目前正在爲西門子等企業做貼牌代工的中國廠商,能否也像九安醫療一樣直接進入美國市場?據公開信息,東方生物(688298.SH)和艾康生物已爲西門子等廠商代工生產快速檢測試劑,此外,美康生物(300439.SZ)、博拓生物(688767.SH)、萬孚生物(300482.SZ)等公司生產的快速檢測試劑,也正申請美國FDA認證。劉毅表示,最終這取決於EUA證書是誰的,如果只是代工而不能自己拿到EUA,則難以成行。九安醫療此次成功,也並非一蹴而就,而是此前公司在美國市場近十一年積累造就的。
春節生產不會受影響 工廠門口經常有人蹲守調研
有投資者提出,如果疫情高峯過去,公司在美國市場的可持續性是否將受影響。劉毅表示,公司經營將跟着市場環境走。2020年新冠疫情伊始,公司曾與小米聯合緊急推出額溫計產品,當時也取得爆發式增長,雖然其後市場變爲正常狀態銷售,但額溫計產品創下了良好口碑,目前其在美國市場銷量仍是第一。試劑盒未來形勢也可同理推導。
而此次新冠試劑盒產品,也已讓ihealth品牌在美國家喻戶曉。據瞭解,九安試劑盒產品目前在美官網價格已由原來的17.98美元/盒提高到19.9美元/盒,提價是由於原材料和人工成本上漲,以及新包含入運費所致,公司產品依然是美國市場上最便宜的,且未來價格在公共衛生防疫領域不會輕易調價。劉毅表示,下一步會利用該品牌優勢拓寬更多產品銷售,“這是我們下一步可能會考慮的問題,現在主要還要先把試劑盒這個仗先打完。”
對於目前已簽署的美國訂單,劉毅表示,訂單將按正常交付就可確認收入利潤。根據九安醫療此前公告,其與紐約州衛生部、美國ACC(美國陸軍合約管理指揮部)的合同分別約定了8周、60日內完成全部交貨的期限,這也意味着正式履約即將給九安醫療今年一季度業績帶來影響。
令人關注的是,目前九安醫療所在的天津正處於奧密克戎疫情關鍵期,這是否會影響九安醫療正常生產運營?劉毅表示,此前兩輪核酸檢測和部分廠區位於管控區,給生產帶來一定影響,但天津封閉後將使工人回家過年的情況變少,春節期間公司會盡量留住工人,不影響產能。至於具體產能變化和擴產可能性,劉毅笑稱,目前九安醫療工廠門口已經常有蹲守觀察、實地調研的人,甚至發現有人混進其廠區調研的情況。
對於新冠試劑盒在國內銷售使用的前景,劉毅表示,這必須在該產品取得國內醫療器械許可證後方可開始。此前,九安醫療曾向天津市疫情防控指揮部提交《關於採用家庭自測盒實現奧密克戎新冠防疫1+1的建議》,目前天津市有關部門仍在研究公司方案。關於家庭自測的方式使用,劉毅表示,這並不是診斷工具,而是一個公共衛生防疫防篩工具,目的是通過及時篩查減少傳染風險,核酸仍是主要的診斷工具,此前公司建議的也主要是在封閉小區內提供居家抗原篩查。
值得注意的是,因股價連續漲停,九安醫療也在投資者交流會後發佈補充公告。公司稱美國政府有權隨時因自身因素中止合同,上述含義爲美國政府可以不需要理由在合同的執行過程中要求停止執行,且取消後續的採購,賣方需承擔相應的風險及可能產生的損失。