引爆股價!5家中國藥企獲准仿製默沙東新冠口服藥,影響幾何?企業回應來了
1月21日,5家中國藥企免費獲准生產、仿製默沙東新冠口服藥的消息,引爆相關個股股價。博瑞醫藥20CM漲停,艾迪藥業漲超10%,復星醫藥上漲5.98%;港股維亞生物漲超13%。
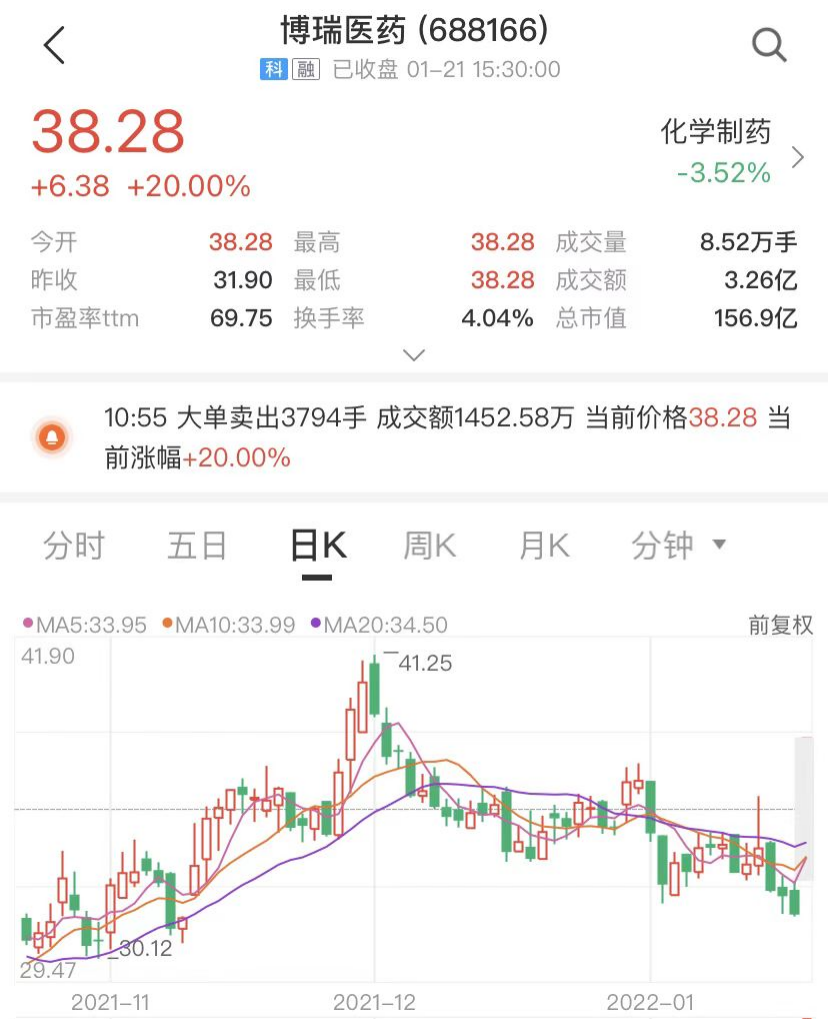
來源:中證金牛座APP
5家中國藥企獲授權
1月20日,由聯合國支持的非營利組織藥品專利池(MPP)公告,與全球27個仿製藥供應商簽訂合約,授權其爲105箇中低收入國家供應默沙東抗新冠小分子治療藥物Molnupiravir。
根據MPP官網,中國符合條件的供應商包括復星醫藥、博瑞醫藥、維亞生物旗下朗華製藥、迪賽諾、龍澤製藥等。其中朗華製藥僅授權供應原料藥,其他國內公司同時授權生產原料藥和製劑。天眼查顯示,上市公司艾迪藥業持有龍澤製藥4.76%的股權。
從商業模式上看,MPP本身並不生產原料藥或仿製藥,由WHO(世界衛生組織)和MPP共同從疾病負擔、有效性、可及性等角度篩選藥品,專利持有方合作授權後,由全球原料藥/仿製藥供應商填寫EOL(意向書),原研廠商可以選擇是否收取特許經營費(如只要新冠肺炎仍被WHO視爲國際關注的突發公共衛生事件,默沙東即不會針對Molnupiravir收取授權費),得到授權的藥企需自己在授權國家推廣銷售。
根據MPP官網,EOL中包含的產能儲備、高質量生產能力、研發能力、法規完備性及財務狀況是MPP考覈的重要標準。
獲授權後多久能上市銷售?
龍澤製藥相關人士稱,這次只是專利授權,不等於獲批。藥品是高監管行業,距離上市還有一段過程。
“拿到授權之後,在藥品上市銷售前,還需要到相應的國家進行註冊,都需要時間。”該人士稱。
該人士表示,公司的產品計劃去熟悉的市場如南非、巴西和俄羅斯進行銷售;此外,巴基斯坦和東南亞後續也會考慮開發。由於產品上市,需要到相應的國家去註冊,由於各個國家對藥品上市的規定不一樣,因此上市的時間也不一致。有的國家可能會很快,尤其是疫情嚴重的國家可能會有綠色通道。
公司在提交上市申請前,還需要做一系列的上市前準備。龍澤製藥相關人士表示:“公司的原料技術包已經具備,製劑的處方工藝相對簡單一些,但是做完後,正常也要做相應的穩定試驗,待收集數據後再提交申請,正常情況下,我們的研發即便再快,也要8-10個月的時間。”
對相關公司影響幾何?
龍澤製藥相關人士稱,目前印度已經有相關產品的指導價,每天治療成本爲18美元左右。“大概率而言,各個國家更像是一個招標市場,初期利潤會大些。”
該人士稱,這次獲批的仿製藥公司就這麼多家,第一家上市銷售的公司價格可能會高,而最後一個上市銷售的企業,應該會是最低價。在他看來,一開始上市銷售的產品,定價會是一種市場行爲。
博瑞醫藥今日公告提示風險稱,本次許可爲非獨家許可,獲許可區域爲印度、巴基斯坦、科特迪瓦等105箇中低收入國家/地區,不包括中國。該產品定價預計將低於原研產品或在其他中高收入國家的售價,具體價格及生產成本等暫無法確定,對未來的業績影響尚無法預計。
浙商證券認爲,獲得MPP授權是一家公司具備全球合規生產能力的一種體現。受益於中國化工配套優勢和合規產能加速擴張,預期中國原料藥和CDMO(定製研發生產)公司在全球藥品供應鏈中影響力加深。從原料藥和製劑國際化角度看,得到授權後公司的銷售額取決於各公司國際銷售網絡搭建和供應鏈管理能力。






