國內專利保護規則日趨細化 藥企、器械商競爭格局生變
摘要:藥品專利保護期限補償制度,是爲了彌補創新藥爲獲得上市批准而造成的有效專利期(從產品上市起的市場獨佔期)的損失而適當增加專利保護期限的制度,主要是爲了彌補因臨牀試驗、審批流程所耗費的一段時間。“藥品專利鏈接制度將明確原研藥企、仿製藥企的競爭規則,兩者間的博弈將成爲常態,藥品專利無效宣告的概率將加大。
原標題:國內專利保護規則日趨細化,藥企、器械商競爭格局生變
加強醫療衛生領域的知識產權保護,不但能夠鼓勵藥企和器械商進行創新,而且能令新技術、新產品在法治規則的不斷細化下加速發展。
今天(4月26日)是第20個世界知識產權日,而今年也是國家專利法實施35週年。
醫療衛生領域的專利權在知識產權中佔據着重要地位。國家知識產權局局長申長雨在23日國新辦發佈上也表示,國家知識產權部門將加快推進專利法修改,建立藥品專利保護期限補償制度。
“我國醫藥產業正逐漸由完全仿製向仿製與創新並舉過渡。目前,我們在生物藥領域有望彎道超車,藥品專利鏈接制度的建立也是自身內在需求。”滙業律師事務所律師王函對第一財經記者表示。
接下來,藥品、器械的知識產權如何進一步得到保障,相關法律文件的指引作用體現在哪些方面,這是否會影響到國內藥企、器械商改變戰略佈局?第一財經記者採訪該領域專家進行詳細解讀。
何爲“專利鏈接”
藥品專利鏈接制度,是指藥品審評審批與藥品專利保護互相“鏈接”的一項制度設計。即仿製藥企業提出仿製藥上市申請時,審批部門需考慮與藥品有關的專利情況,避免批准侵犯專利權的藥品上市。
儘管我國還未建立與美國類似的藥品專利鏈接制度,但在一些法律文件中已有相關具有約束力的規定。
比如,在此前的《藥品註冊管理辦法(修訂草案徵求意見稿)》起草說明裏提到,“42號文件(即《關於深化審評審批制度改革鼓勵藥品醫療器械創新的意見》)提出探索建立藥品專利鏈接制度。該制度的核心目的是儘量減少仿製藥審批中潛在的專利糾紛。專利鏈接制度涉及藥品專利權人和仿製藥企業的利益,以及對藥品可及性和公共健康產生影響。”
再如,新修訂的《藥品註冊管理辦法》也對符合豁免藥物臨牀試驗條件的申請人作出了仿製藥簡化申請(ANDA)的規定;《藥品管理法實施條例》中對於創新藥數據保護期也給予了6年的期限,但公共利益需求等除外。
而《專利法》69條則詳細闡述了不構成侵犯專利權的行爲;如提供行政審批所需要的信息,製造、使用、進口專利藥品或者專利醫療器械等都不視爲侵犯專利權。
建立藥品專利鏈接制度,將對我國藥企帶來哪些影響?王函認爲,該制度一方面保護了原研藥專利權,另一方面還能激發仿製藥的積極性,在首仿藥、創新藥兩方面持續創新。
詳細來說,如果原研藥企業在可能侵權的仿製藥獲得上市許可前提起專利訴訟,那麼其被侵權的風險也將隨之降低;有的原研藥企爲了自身藥品專利不被輕易挑戰成功,其在研發過程中會更加註重創新,並完善專利佈局。
“以瑞德西韋爲例,吉利德爲該創新藥物申請57個同族專利進入57個國家,涉及合成方法、結構類似物、劑型、絲狀病毒、黃病毒、正黏病毒科等。此外,吉利德還將瑞德西韋用於冠狀病毒申請了專利,這也對武漢病毒所後續專利申請授權帶來不小威脅。”王函補充。
而按照我國現有藥品上市審批程序,如果原研藥專利權人主張其專利權,藥品審批部門將會等到專利期屆滿後再審批仿製藥,藥企間產生衝突的可能性很小。
“藥品專利鏈接制度將明確原研藥企、仿製藥企的競爭規則,兩者間的博弈將成爲常態,藥品專利無效宣告的概率將加大。未來,藥品專利分析、相關糾紛案件數量也將大幅上升。”王函說。
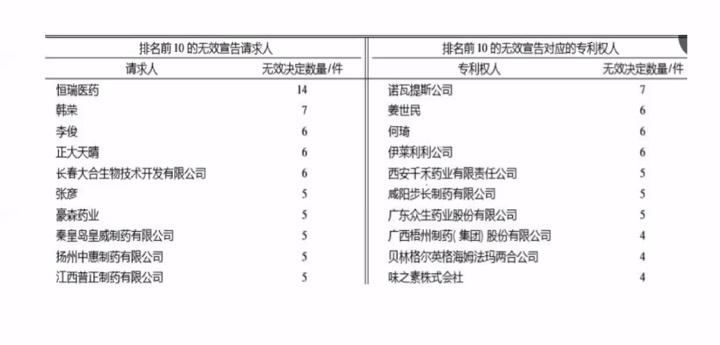

2008~2017 年國內醫藥領域專利無效宣告決定情況。圖片由滙業律師事務所提供
而在此背景下,最高院出臺《最高人民法院2020年度司法解釋立項計劃》將“關於審理藥品專利鏈接糾紛案件適用法律若干問題的規定”作爲新立項的司法解釋要求在2020年底前完成。
專利保護期限補償
在藥品專利權的系統性保障下,“藥品專利保護期限補償“制度是業界聚焦重點。
藥品專利保護期限補償制度,是爲了彌補創新藥爲獲得上市批准而造成的有效專利期(從產品上市起的市場獨佔期)的損失而適當增加專利保護期限的制度,主要是爲了彌補因臨牀試驗、審批流程所耗費的一段時間。
2017年10月公佈的42號文件,就提到了要“開展藥品專利期限補償制度試點”。
2019年1月,在我國《專利法》修正案中關於創新藥專利期限延長的部分提到,“對在中國境內與境外同步申請上市的創新藥品發明專利,國務院可以決定延長專利權期限,延長期限不超過5年,創新藥上市後總有效專利權期限不超過14年。”
“對於國內藥企而言,藥品專利的佈局需要上升到戰略層面,需要思考如何去應對原研藥已佈局好的專利網,比如說逐漸向高層次的仿製、首仿靠攏,摒棄仿製一些已經淘汰的、沒有專利的藥品。”滙業律師事務所唐嘉偉律師告訴記者,“政策制定需要在原研藥、仿製藥兩者間作平衡與兼顧,國內仿製藥應利用原研藥專利到期的點,讓藥物及早上市、儘快盈利,這是非常重要的。”
唐嘉偉建議,藥企也要充分了解政策並利用好制度組合拳。儘管該制度上會更偏向於原研藥,但同時也在鼓勵仿製藥向原研藥進行挑戰,這也是對高質量仿製藥企的倒逼。
此外,此次疫情也使《專利法》中關於“藥品專利強制許可”制度頻頻被提及。
藥品專利的強制許可,包括爲實施或者未充分實施的強制許可、構成壟斷行爲時的強制許可、爲公共利益的強制許可、爲公共健康的出口的藥品強制許可、從屬專利的強制許可。
“在過往實踐中,藥品專利的強制許可幾乎沒有被用到過,但新冠病毒讓大家重新探討這一制度的可能性。”唐嘉偉說,“以從屬專利的強制許可來說,儘管武漢病毒研究所的專利被授權,但原研藥瑞德西韋新冠適應症的專利在更上游。那麼一旦發生類似事件,武漢病毒研究所的專利其實還是能夠順利實施的,只是採用的邏輯是強制許可。”


圖片由滙業律師事務所提供


圖片由滙業律師事務所提供
提升發明專利質量
申長雨在4月23日還表示,要通過加大知識產權保護力度,促進醫療行業創新發展,研發出更多創新藥和精密醫療器械,提高救治能力和水平。
根據《健康產業專利態勢分析報告》的數據,截至2020年4月10日,全球健康產業專利申請公開874萬餘件,中國健康產業專利申請258萬餘件,佔比29.6%居全球首位。
奧諮達醫療器械服務集團的數據顯示,2008~2017年全球醫療器械專利申請量約200萬件,中國在這10年間共申請專利超62萬件,專利數量從2008年的28588項到2017年67422項,已超過全球總量50%。
“我國醫療器械專利活躍度已經超過美國及一些世界先進國家。雖然我國器械專利申請快速增長,但是發明專利的新穎性、創造性一直不足,如何提高專利質量是醫療器械領域面臨的重要課題。在國外,專利申請人大部分都是大型企業,而我國則主要以高校及國外專利爲主。”奧諮達醫療器械服務集團東區市場總經理詹金城對記者表示。
由此可見,我國醫療器械仍處於仿製及向創新轉變的初步階段,需要更多企業來發明高質量的核心專利。
專利糾紛也是器械商需要尤其注意的層面。“我國早期仿製國外高端產品,但由於很多高端設備專利無法完全仿製,故發明出來的產品與國外常有較大性能差異。但由於國內內需市場巨大,當產品賣出一段時間後,原廠發覺市場被瓜分,於是在國外提出告訴,企業資金被凍結造成資金運轉不靈。”詹金城認爲。
醫療衛生領域知識產權的司法環境如何,法律怎樣保障企業權益?上海知識產權法院相關法官告訴記者,“目前醫療衛生領域中,涉案專利技術包括中醫藥製備技術、基因檢測、原料藥和植入性醫療器械等。這些專利技術普遍比較複雜,與該領域前沿技術發展息息相關。”
“爲此,法院首先要解決的是權利人舉證難題;其次,醫療衛生領域案件涉案技術較爲複雜,要有效運用多元化技術以及專家陪審等方式事實查明機制。再次,由於醫療衛生領域涉案技術價值普遍較高,案件審理中充分考慮涉案專利權的類型、侵權人侵權行爲性質、侵權持續時間、後果及專利貢獻度等因素,因此,要依法適用有利於權利保護的賠償計算方式。”該法官表示。