白雲山子公司天心藥業注射劑檢出可見異物 曾被收回GMP證書
原標題:白雲山子公司天心藥業注射劑檢出可見異物 曾被收回GMP證書
中國經濟網北京4月8日訊(記者朱國旺 郭文培) 繼被收回GMP證書後,白雲山旗下廣州白雲山天心製藥股份有限公司藥品再現質量缺陷。日前,上海市藥品監督管理局發佈的《2021年第1期藥品質量抽檢通告》顯示,經上海市食品藥品檢驗所檢驗,標示廣州白雲山天心製藥股份有限公司生產的注射用頭孢呋辛鈉(批號:200816)檢出可見異物。

可見異物係指注射劑、眼用製劑中,在規定的目視條件下能夠觀察到的不溶性物質,該項目不符合規定可能造成局部循環障礙等用藥安全風險。
值得注意得是,不久前,廣州白雲山天心製藥股份有限公司剛因生產管理不符合規定被收回GMP證書。2018年12月5日,國家藥監局發佈《對廣州白雲山天心製藥股份有限公司跟蹤檢查通報》稱,在對廣州白雲山天心製藥股份有限公司跟蹤檢查中發現,該公司存在直接接觸藥品的容器未經批准、未驗證用於部分批次的產品生產等多項問題,同時注射用鹽酸頭孢甲肟的生產質量管理不符合《藥品生產質量管理規範(2010年修訂)》相關規定,責成廣東省藥品監督管理局收回該企業相關藥品GMP證書,並進一步調查處理。

另據中國質量新聞網,廣州白雲山天心製藥股份有限公司曾多次上榜藥品不合格名單。比如,浙江省食品藥品監督管理局發佈的《2007年第5期浙江省藥品質量公告》顯示,標示廣州白雲山天心製藥股份有限公司生產的注射用頭孢呋辛鈉(批號:060902)不合格,不合格項目爲溶液的顏色。江西省食品藥品監督管理局發佈的《2010年江西省藥品質量公告(基本藥物抽驗專期第4期)》顯示,標示廣州白雲山天心製藥股份有限公司生產的克林黴素磷酸酯注射液(批號:100306)不合格,不合格項目爲可見異物。


公開資料顯示,廣州白雲山天心製藥股份有限公司爲白雲山控股子公司。白雲山日前披露的《2020年年度報告》顯示,廣州白雲山天心製藥股份有限公司註冊資本4569.31萬元,白雲山間接持股82.49%。

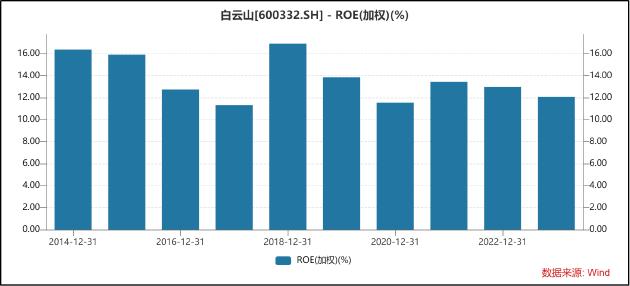
值得注意的是,2020年白雲山業績也遭遇滑鐵盧,公司營收淨利10年首次雙降。其中,實現營收616.7億元,同比下降5.05%;歸屬淨利潤29.15億元,同比下降8.58%。