PD-1“出海”迎突破,难敌诺华再度“退货”担忧,百济神州单日跌超4%
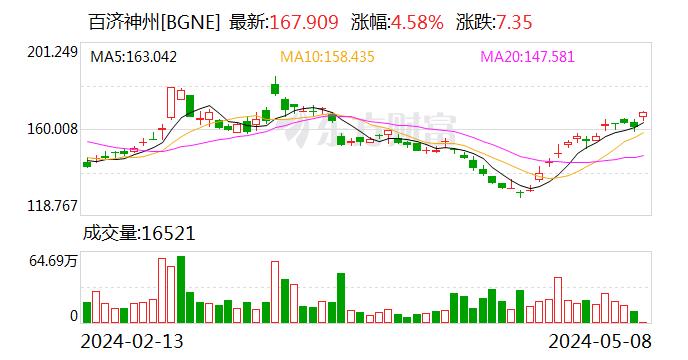
9月20日,百济神州(688235.SH,06160.HK)A股和港股双双开盘下跌,当日A股报收138.9元/股,跌幅4.09%,港股报收121港元/股,跌幅4.72%。看起来,即便公司的PD-1产品替雷利珠单抗出海迎来突破,投资者还是更多的展现出了对其终止与诺华就该产品的合作的担忧。
继TIGIT靶点药物后,与诺华合作再终止
9月19日晚,百济神州公告,公司的全资间接子公司百济神州瑞士和诺华共同终止替雷利珠单抗的授权协议,协议生效后,百济神州瑞士重新获得开发、生产和商业化替雷利珠单抗的全部全球权利,且无需支付特许使用费。
围绕授权协议终止后的安排,公告显示,诺华可以继续开展正在进行的临床试验,并且未来在获得百济神州同意后可以开展其他替雷利珠单抗联合用药试验。百济神州同意继续为诺华提供替雷利珠单抗的临床试验用药,以支持其临床试验的开展。根据协议,诺华将向百济神州提供过渡服务以确保替雷利珠单抗开发和商业化计划中的关键事项顺利推进,包括对生产、药政申报、药品安全和临床事项的支持。
百济神州还指出,此次终止不会影响百济神州瑞士前期已从诺华收到的6.5亿美元的现金首付款,亦不会对公司的财务状况和经营状况产生重大不利影响。
替雷利珠单抗是百济神州自主研发的人源化igg4抗PD-1单克隆抗体,设计目的旨在最大限度地减少与巨噬细胞中的Fcγ受体结合,帮助人体免疫细胞识别并杀伤肿瘤细胞。
百济神州与诺华就替雷利珠单抗的合作始于两年多前。2021年1月,百济神州瑞士和诺华签订协议,百济神州瑞士授予诺华在美国、加拿大、墨西哥、欧盟成员国、英国、挪威、瑞士、冰岛、列支敦士登、俄罗斯和日本开发、生产和商业化tislelizumab(替雷利珠单抗)的权利。根据授权协议,诺华负责在授权国家的注册申请,并有权在获批后开展商业化活动。
值得注意的是,有关百济神州和诺华围绕替雷利珠单抗的授权合作终止的担忧,早在两个月前诺华终止与百济神州有关欧司珀利单抗的合作时就已出现。7月,两家公司签署终止协议,终止了在2021年12月签订的《选择权、合作和许可协议》,在这份协议中两家公司曾约定,百济神州瑞士授予诺华一项独家的、基于时间的选择权,以使诺华可以通过行使该选择权获得在若干国家和地区开发、生产和商业化公司的在研TIGIT抑制剂欧司珀利单抗(ociperlimab)的独家许可。
TIGIT与PD-1的组合被认为在提高药效的同时,还有望降低毒副作用,产生“1+1>2”的效果,目前除了百济神州外,还有不少头部创新药企也在这一靶点布局。因此欧司珀利单抗与替雷利珠单抗的联用被市场寄予厚望。然而诺华对欧司珀利单抗的“退货”引发市场对TIGIT靶点开发是否能成功的担忧,同时也为替雷利珠单抗能否顺利出海增加了不确定性。毕竟在海外PD-1市场,默沙东的K药、BMS的O药等已获批大适应症的情况下,如果与TIGIT药物的联用确实能增强替雷利珠单抗的效果的话,替雷利珠单抗在海外销售的前景会乐观许多。
事实证明上述担忧并非毫无道理。眼下诺华确实终止了就替雷利珠单抗与百济神州的合作,百济神州因此重新获得替雷利珠单抗的全部全球权利。对于诺华终止替雷利珠单抗的合作是否和此前终止就欧司珀利单抗的合作有关,银柿财经询问了百济神州方面,对方回复称:“这次仅涉及替雷利珠单抗,不受欧司珀利单抗相关协议的影响。”
与上述消息一同宣布的还有布替雷利珠单抗获得欧盟上市批准,以及上市申请获美国FDA受理的消息。公告显示,欧盟委员会已批准百泽安 (替雷利珠单抗)作为单药用于治疗既往接受过含铂化疗的不可切除、局部晚期或转移性食管鳞状细胞癌(ESCC)的成人患者。
另外,美国FDA已受理百泽安 的一项上市许可申请,用于一线治疗不可切除的局部晚期、复发或转移性的ESCC患者。根据《处方药使用者付费法案》(PDUFA),美国FDA预计将在2024年下半年对该项申请做出决议。
“权益收回”亦是“退货”
对诺华选择终止替雷利珠单抗合作协议的原因,百济神州方面透露,诺华之所以同意把权益交还,是因为诺华最近战略上有很多调整,在“聚焦”调整框架下,这是对双方及产品都更为有益的一大决策。
在百济神州官方公众号发布的推文中,公司强调“权益的收回”,而在投资者看来,这也是被诺华“退货”。

来源:百济神州官方微信公众号
来源:网络

来源:网络
投资者担忧,诺华方面是否对替雷利珠单抗在海外的销售前景不再看好。在被问及公司如何评估这一情况时,百济神州方面向银柿财经提供一份资料,百济神州看起来对这项产品的商业化仍充满信心。
据上述资料,百济神州以泽布替尼为例说明公司具备的全球自主商业化能力。泽布替尼是百济神州首款在国际市场获批的创新药,目前泽布替尼已在全球超过65个市场获批。
另外,临床前研究表明,相较其他同类药物,替雷利珠单抗与PD-1的亲和力或许更高,可能源于其特有的PD-1结合方位。在国内,目前,替雷利珠单抗获国家药品监督管理局(NMPA)批准11项适应症,其中9项适应症纳入国家医保目录,是国内获批适应症最广泛、纳入医保适应症数量最多的PD-1产品。2023年上半年,替雷利珠单抗在中国的销售额总计18.36亿元,相较于2022年同期12.51亿元的销售额,同比增长超过了四成。百济神州方面认为,此次替雷利珠单抗在欧盟获得批准,也印证了替雷利珠单抗强大的产品实力。
但与此同时,招银国际分析师指出,鉴于消化道肿瘤在欧美发病率不高,预期替雷利珠未来销售收入仍将主要来源于国内。
由此来看,尽管替雷利珠单抗摘得国内首个出海的PD-1“桂冠”,百济神州这一产品未来的商业化进程仍然路漫漫。终止与诺华的合作后,公司也提到未来不排除选择与其他公司有所合作。相关进展还需持续关注。