君實生物VV116上市申請獲受理,國產新冠口服藥加速“闖關”
來源:21世紀經濟報道
臨牀前研究顯示,VV116對包括奧密克戎在內的新冠病毒原始株和突變株表現出顯著的抗病毒作用,且無遺傳毒性。
21世紀經濟報道記者 季媛媛 上海報道 繼先聲藥業先諾欣 (先諾特韋片/利托那韋片組合包裝)新藥上市申請(NDA)獲國家藥監局(NMPA)以藥品特別審批程序受理後,1月17日,君實生物宣佈,NMPA已受理公司旗下的口服核苷類抗新型冠狀病毒(SARS-CoV-2)藥物氫溴酸氘瑞米德韋片(產品代號:VV116/JT001)新藥上市申請(NDA),用於新型冠狀病毒感染(COVID-19)的治療。
VV116是一款新型口服核苷類抗病毒藥物,能夠以三磷酸形式非共價結合到新冠病毒RNA聚合酶的活性中心,直接抑制了病毒RNA聚合酶的活性,阻斷子代病毒的複製,從而實現抗病毒的作用。臨牀前研究顯示,VV116對包括奧密克戎在內的新冠病毒原始株和突變株表現出顯著的抗病毒作用,且無遺傳毒性。
有證券機構醫藥行業分析師對21世紀經濟報道分析指出,目前,儘管國內已有三款新冠口服藥獲批上市,但包括藥物安全性、有效性、可及性等多種因素導致藥物的應用受限,因此還需要研發更多療效及安全較高的治療藥物。從現有的研究結果來看,VV116具備強勁的商業化潛力,這款藥物有望爲我國乃至全球新冠患者提供效果更好、更安全的治療選擇。
“新冠疫情感染率的控制仍舊將以疫苗爲主,未來整體新冠口服藥的研發仍將以降低死亡率爲首要的目標,同時最大程度上減輕症狀。近期的藥物研發主要以奧密克戎的特性做臨牀研究,而新冠病毒屬於RNA病毒,基因突變的概率高,長期的變化大,未來的口服新冠藥需要考慮潛在的突變毒株,進行作用機制的改進,因此也將有更多靶點的口服新冠藥物加入到研發格局當中。”該分析師說。
VV116療效究竟如何?
根據君實生物官方資料,2021年11月,VV116的新藥臨牀試驗申請(IND)獲得NMPA批准。隨後開展的3項I期臨牀研究顯示,VV116表現出令人滿意的安全性、耐受性和藥代動力學性質,口服吸收迅速。
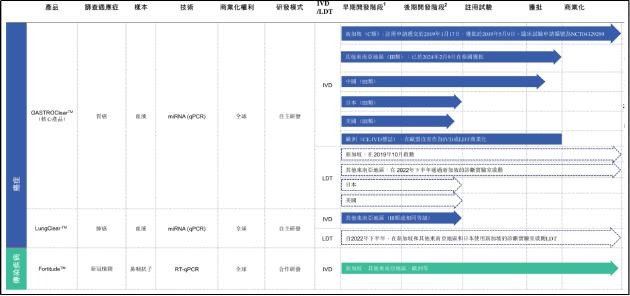
一項VV116對比奈瑪特韋片/利托那韋片組合包裝(PAXLOVID)用於伴有進展爲重症(包括死亡)高風險因素的輕中度COVID-19患者早期治療的III期臨牀研究(NCT05341609)主要終點達到設計的非劣效終點,相比PAXLOVID,VV116組的臨牀恢復時間更短(4天 vs. 5天),安全性方面的顧慮更少。該研究成果獲得全球權威期刊《新英格蘭醫學雜誌》(The New England Journal of Medicine,NEJM,影響因子:176.079)發表。
2022年10月21日,一項在伴或不伴有進展爲重症高風險因素的輕中度COVID-19患者中評價VV116有效性和安全性的多中心、雙盲、隨機、安慰劑對照、III期臨牀研究(NCT05582629)完成首例患者入組及給藥。該研究由浙江大學醫學院李蘭娟院士牽頭,在全國32家中心開展。該研究已完成方案預設的期中分析,經獨立數據監察委員會(IDMC)判定已達成方案預設規定的主要有效性終點。關於詳細的研究數據,君實生物方面稱將在後續公佈。
針對VV116的治療效果,中科院院士丁健教授曾在解讀VV116 “頭對頭”輝瑞Paxlovid臨牀試驗結果時指出,抗新冠病毒藥物是有效應對疫情的重要手段之一,尤其是我國在疫情有效防控取得積極重大成果的基礎上,出臺“二十條”優化措施和疫情防控“新十條”,實施疫情更加科學精準防控,更加需要加強抗新冠藥物的研發、生產和儲備。口服小分子抗新冠病毒藥物具有使用方便、可及性好等方面的優勢,將在當前和今後疫情防控中發揮重要作用。
“RNA複製酶作爲病毒轉錄複製的核心組件,是抗新冠病毒藥物研發的重要靶標之一,且其功能在病毒變異中高度保守,針對此靶標研發的抗新冠病毒藥物不易受病毒變異的影響。臨牀前研究和1期臨牀研究,已經確證了VV116抗新冠病毒的活性和安全性,該項VV116與Paxlovid口服治療Covid-19比較的臨牀研究,進一步驗證了VV116治療奧密克戎變異株感染患者的有效性和安全性。”丁健教授說。
中日友好醫院副院長、呼吸與危重症醫學科主任曹彬教授也指出,突發公共衛生事件下開展臨牀試驗本身就面領諸多困難,尤其是需要與疫情搶時間,在暴發窗口期完成新藥的效力驗證,最爲關鍵的就是快。這樣的臨牀試驗結果將爲後續該傳染病再次暴發或者大流行提供重要的參考價值。
不過,此次關於VV116究竟何時進入臨牀應用,君實生物方面並未做出相關回應。
國產新冠口服藥競爭加劇
根據21世紀經濟報道記者梳理,目前,全球已經上市的主要新冠治療藥物包括輝瑞的Paxlovid(口服),默沙東的Molnupiravir(口服)、吉利德的Remdesivir(注射)以及真實生物的阿茲夫定(口服)等。上市申請獲得NMPA受理的企業包括君實生物及先聲藥業,此外,國內還有10多個處於臨牀研發階段的新冠口服藥,涉及企業包括開拓藥業、亞盛醫藥、衆生藥業、歌禮制藥、雲頂新耀、綠葉製藥、復宏漢霖、神州細胞等。
安信證券認爲,根據藥企相關新冠藥物的臨牀開發進度,上半年將有多個藥物獲批上市。總的來看,先聲藥業SIM0417、君實生物VV116、衆生藥業RAY1216成爲了業內看好的種子選手 。
其中,先聲藥業SIM0417研發進度已經處於國內3CL靶點領先位置,且研究數據顯示,SIM0417對包括德爾塔毒株在內的多種新冠變異毒株均有很強的抑制作用。
同時,衆生藥業爲國內第二家獲批III期臨牀的3CL靶點小分子新冠藥物,華鑫證券1月3日研報指出,III期臨牀試驗主要終點爲28天臨牀症狀的持續改善,考慮到作爲新冠治療用藥可納入藥監局的特別審批程序上市, 預計2023年Q1將完成III期臨牀試驗及EUA申請相關工作 。
至於此前與君實生物幾乎處於同一起跑線的開拓藥業普克魯胺也備受關注。重慶市腫瘤醫院泌尿外科主任醫師羅宏在接受21世紀經濟報道記者採訪時表示,普克魯胺在治療新冠方面的不錯效果,它主要是通過下調ACE2和TMPRSS2減少病毒感染宿主細胞,以及免疫調控。在這次新冠暴發的時候,我們也在觀察該藥物的安全性。畢竟,任何藥物應用於新冠治療,安全性也是主要考慮問題,還有是否會導致對雄激素的抑制,是否有生殖安全性問題。
“我們在對抗雄藥物的研究發現,普克魯胺作用的是雄激素受體,而非對雄激素進行抑制,甚至在臨牀上觀察到短期類似普克魯胺新型抗雄藥物還會帶來雄激素的上調,新型抗雄藥物深度抑制雄激素受體,導致雄激素一定程度的上調,理論上是成立的,所以短期用藥更不會引起生殖毒性。即便針對前列腺癌晚期患者,普克魯胺藥物的長期使用其安全性也是良好的。 ”羅宏教授說。
據悉,開拓藥業已完成在美國等國家進行的普克魯胺治療輕中症新冠患者III期全球多中心臨牀試驗,結果顯示普克魯胺可有效降低新冠患者住院/死亡率。目前開拓藥業正在積極推進普克魯胺在中美等國家的緊急用藥批准/緊急使用授權(EUA)。
目前,在投入大量資金佈局後,新冠治療藥物的市場前景也成爲業內外人士關注的重點話題。
CIC灼識諮詢總監劉立鶴對21世紀經濟報道記者表示,在這樣的流行趨勢下,臨牀上對新冠藥物的潛在需求會持續增長,並且需要機制和療效的創新改進以降低死亡率的數據,同時也需要爲奧密克戎以外的其他類型的毒株做準備。
那麼,對於臨牀試驗進展相對較緩慢的企業而言,應該如何緊抓市場佈局?上述分析師指出,變異病毒株的流行造成全球住院患者數持續攀升,全球中、重度住院患者高危人羣對抗新冠病毒藥物有長期、剛性的需求。
“新冠口服藥的整體研發仍將以降低死亡率爲首要目標,同時最大程度減輕症狀。未來的口服新冠藥需要考慮潛在的突變毒株,進行作用機制的改進,因此也將有更多靶點的口服新冠藥物加入到研發格局當中。”劉立鶴強調。