單日爆天量瘋漲54%引關注!雲頂新耀離盈利還有多遠?

6月15日,在港上市的生物科技公司大多迎來上漲,其中啓明醫療-B(02500.HK)、加科思-B(01167.HK)、和鉑醫藥-B(02142.HK)均漲超10%。
不過,板塊內表現最佳的其實還是雲頂新耀-B(01952.HK),該股日內放出天量瘋漲了54.01%,漲幅高居全市場首位。
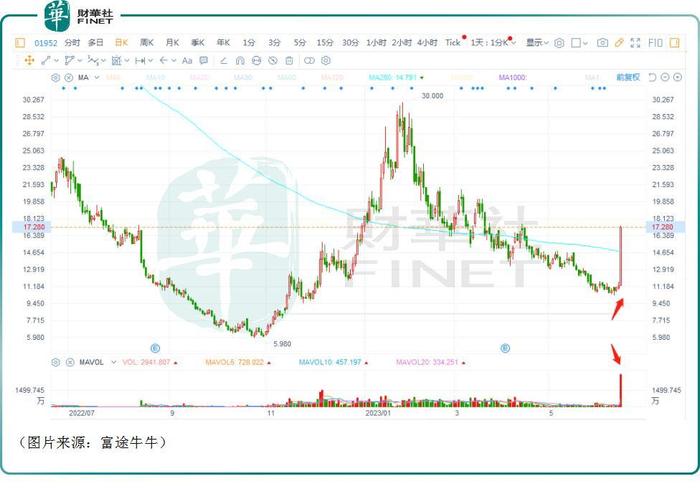
結合成交量、股價漲幅、分時走勢來看,雲頂新耀顯然獲得了市場資金的力挺,這也引起了投資者的高度關注。
一款主要產品持續迎來利好
雲頂新耀於2020年10月登陸港交所,公司是一家專注於後期臨牀階段的生物製藥公司,致力於在全球範圍內引進專利許可,開發和商業化創新性療法,其在腎科疾病、mRNA平臺、感染性和傳染性疾病、自身免疫性疾病等領域已建立全球同類首創或者同類最佳的藥物和疫苗組合,如下圖所示。

值得注意的是,雲頂新耀於6月15日迎來股價的“狂飆時刻”,從消息面來看,該公司旗下的一款主要產品Nefecon(耐賦康)在最近幾個月頻頻傳來利好,這也被一些投資者視爲是股價大漲的原因之一。
Nefecon(耐賦康)是口服靶向布地奈德遲釋膠囊,作爲全球唯一對因治療IgA腎病的治療藥物,是靶向腸道的黏膜免疫調節劑,能減少50%腎功能下降,延緩超過10年進展至透析或腎移植。布地奈德是一種具有強糖皮質激素活性和弱鹽皮質激素活性的糖皮質激素,首過代謝程度達90%,具有良好的安全性。Nefecon專爲IgA腎病患者研製,遲釋膠囊含布地奈德4mg,通過特殊的製作工藝,將布地奈德靶向釋放於迴腸末端的黏膜B細胞(包括派爾集合淋巴結),膠囊溶解後,三層包衣微丸持續穩定釋放布地奈德,高濃度覆蓋整個靶區域,從而減少誘發IgA腎病的半乳糖缺陷的IgA1抗體(Gd-IgA1)產生,進而干預發病機制上游階段,達到治療IgA腎病的作用。
據瞭解,這款產品也是雲頂新耀引進的。2019年6月,該公司與Calliditas簽訂獨家授權許可協議,獲得在大中華地區和新加坡開發以及商業化Nefecon的權利。2022年3月,經擴展後,韓國也被納入了授權許可範圍。
從進展來看,2022年11月,Nefecon(耐賦康)的新藥上市許可申請(NDA)已被中國國家藥品監督管理局納入優先審評,還在中國作爲首款非腫瘤藥物被納入突破性治療品種,預計2023年下半年在中國內地獲批上市。中國臺灣地區藥政部門也於2022年11月授予Nefecon加速覈准機制(AAD)認定。
2023年4月,新加坡衛生科學局(HSA)已受理Nefecon(耐賦康)的新藥上市許可申請(NDA),Nefecon(耐賦康)預計於2023年內在新加坡獲批上市。同月,有消息報道稱,Nefecon(耐賦康)已獲得海南省藥品監督管理局批准,將在上海交通大學醫學院附屬瑞金醫院海南醫院應用於臨牀使用。
此外,韓國食品醫藥品安全部(MFDS)將Nefecon(耐賦康)作爲首款非腫瘤產品納入全球創新產品快速通道(GIFT)計劃。納入GIFT計劃後,預計可將審批時間縮短25%,並允許進行滾動審理。
多年來持續虧損,“賣資產”後虧損大幅收窄
雖然說Nefecon(耐賦康)已經非常接近商業化上市,但在當下雲頂新耀旗下畢竟仍沒有商業化上市的產品,這也導致了該公司是一個還未盈利的狀態,這一點和百濟神州(06160.HK)、君實生物(01877.HK)等同行是一樣的。
數據顯示,雲頂新耀多年來一直處於虧損之中,2020年暴虧了56.58億元(如非特指,以下元均指人民幣),而自那之後其虧損在逐漸收窄,2022年僅虧損了2.47億元。
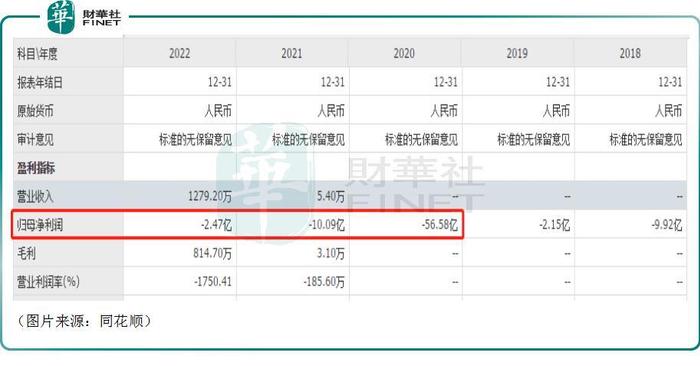
需要指出的是,2022年虧損大幅收窄有一些偶然因素。
據悉,2019年4月,雲頂新耀以8.35億美元的合作價從原研企業Immunomedics處獲得戈沙妥珠單抗在大中華地區及部分亞洲國家的開發、註冊及商業化權益。
戈沙妥珠單抗是一款FIC的TROP-2ADC,在中國內地獲批3L+TNBC(三陰性乳腺癌)適應症。
到了2022年6月,戈沙妥珠單抗已經獲批在國內上市,即將開始商業化。此時,雲頂新耀已支付1.25億美元首付及里程碑付款,剩餘至多7.1億美元里程碑付款。
不過,兩個多月後,雲頂新耀就選擇以4.55億美元的對價將戈沙妥珠單抗亞洲權益轉讓給了吉利德科學(GILD.US)。具體而言,4.55億美元對價,包括2.8億美元首付款和潛在1.75億美元里程碑付款;同時,原許可協議將被終止。
這件事在當時引起了很多質疑,該公司的股價也在當日暴跌了19%,並在隨後開啓了一波猛烈的下跌。
雖然爭議不少,但在這筆“買進賣出”的交易中,雲頂新耀是賺了一筆的,對其業績減虧起到了比較大的作用。
兩款產品商業化在即,雲頂新耀距盈利還有多遠?
而在賣了戈沙妥珠單抗之後,雲頂新耀當下最具有看點的產品就是上述的Nefecon(耐賦康)和依嘉®(依拉環素)。
依嘉®(依拉環素)是全球首個氟環素類抗菌藥物,用於治療常見的革蘭陰性菌、革蘭陽性菌、厭氧菌等包括多重耐藥菌的感染。依拉環素是雲頂新耀從Tetraphase製藥公司(現爲Innoviva,Inc.的全資子公司)授權引進,擁有大中華區、韓國、東南亞的商業化權益。
2023年3月,中國國家藥品監督管理局批准依嘉®用於治療成人患者複雜性腹腔內感染的新藥上市許可申請(NDA)。至此,依嘉®已在美國、歐盟、英國、新加坡、中國內地和中國香港被批准用於治療複雜性腹腔內感染。依嘉®中國臺灣地區治療複雜性腹腔內感染的新藥上市許可申請(NDA)正在審理中,預計將於2023年獲批。
西部證券預計依嘉®(依拉環素)將於2023年三季度啓動中國商業化。
基於現有的產品管線及研發、商業化進展,該機構還預計,雲頂新耀2023-2025年營收分別爲4.52/6.04/15.74億元,同比增長3433%/33.7%/160.5%;歸母淨利潤分別爲-4.10/-2.45/2.46億元。
也就是說西部證券預計雲頂新耀能在2025年扭虧爲盈。
當然了,以上只是一家之言,不過隨着上述的兩款產品實現上市銷售,雲頂新耀的業績有望實現大幅增長,距離盈利的目標將更近一步。
結語
值得一提的是,經過漫長的回調之後,雲頂新耀所屬的生物醫藥賽道的投資價值也得到了一些機構的看好。
例如,華安證券就表示,醫藥目前到了很多標的估值能接受、但是苦於沒有板塊行情的機會的階段,資金持續在觀望,稍微拉長時間維度,醫藥目前這個時間點配置,會顯示出很好的投資價值。現在醫藥的投資機會需要自下而上選擇,挖掘具備競爭力和差異化的公司。
後續雲頂新耀會不會延續股價漲勢值得觀察。
作者:燕十四






