17 位學者發表評論文章,討論實驗室腦組織培養帶來的倫理難題
17 位著名的科學家、倫理學家和哲學家在本週《自然》上發表了一篇評論文章,指出現在需要對培養或維持人腦組織的行爲做出倫理考量。舉例來說,如果研究人員有一天可以在實驗室內創造出一個似乎可以產生意識經驗的模型,那麼這是否會引發有關所有權、管理、權限、處置和數據保護方面的問題?
爲了研究帕金森病和精神分裂症等疾病,研究人員正在利用幹細胞培養小型簡化版的人腦組織——腦類器官。另有一些研究人員已經將人腦細胞移植至小鼠身上,還有一些人在研究手術時從患者身上移除的腦組織。這類模型可能具有無窮的價值,“但是腦類器官離功能性人腦越近,倫理問題就越嚴重。”Farahany 等人如此表示。
作者們提出了一些他們認爲研究人員、資助機構、審查委員會和公衆應該加以討論的問題,以便爲這類研究提供指引。這些問題包括研究人員是否有可能評估腦替代品的知覺功能以及人類對於生死的理解可能將受到的挑戰。
作者總結說:“爲了確保這類研究可以在長期範圍內取得成功,併爲社會所接受,現在必須制定一個倫理框架。”他們還指出,人腦實驗模型或有助於解開長期以來令人難以理解的精神疾病和神經疾病謎題。
妮塔·A·法拉赫、亨利·T·格里利和另外 15 名同事表示,當人腦模型越來越接近能複製人腦的功能時,倫理難題會隨之而來。
如果研究人員能夠在實驗室中創造出可能具有意識經驗或主觀思想狀態的腦組織,那麼這些腦組織是否應該受到人類或動物研究對象所能受到的常規保護呢?

利用人體幹細胞作爲起始原料,在培養皿中培養出簡化的 3D 人腦類器官。
Credit: Genome Institute of Singapore, A*STAR
這個問題可能看起來太過古怪。當然,今天的實驗大腦模型遠不具有這樣的能力。但是現在研究人員正在開發各種各樣的大腦模型來更好地瞭解人類的大腦,包括利用幹細胞培養微型簡化版的大腦組織——人腦類器官(brain organoids )。這方面的研究在不斷進步。
這些模型可以比動物模型更精確地表現正常和異常的人類大腦功能和發育(儘管動物模型仍舊可以用於許多其他目的)。現在,一方面神經和精神疾病給人類帶來了巨大痛苦,而依據動物模型開發出來的大多數治療方法都不能在人身上發揮作用,另一方面人類大腦替代物對這個領域來說希望極大,有鑑於此,完全放棄這方面的研究本身看上去似乎就有違倫理。然而,當大腦替代物越接近一個功能正常的人類大腦,這些研究就會變得越有倫理問題。
現在有必要爲這類研究制定明確的指導方針,不過它們可以根據新的科學發現進行調整。這是許多神經科學家、幹細胞生物學家、倫理學家和哲學家——包括我們在內——得出的一個結論,我們在過去的一年裏研究了人腦類器官(brain organoids)和相關神經科學工具所引發的倫理困境。2017 年 5 月,在美國國立衛生研究院(NIH)腦計劃(BRAIN INITIATIVE)的有限支持下,一場研討會在杜克大學的科學與社會倡議組織(Duke Initiative for Science & Society)內如期舉行。而上個月,在美國又舉行了一次類似的會議,來討論相關議題。
在這裏,我們列出了一些我們認爲研究人員、資助者、審查委員會和公衆應該討論的問題,作爲指導大腦替代物研究的第一步。
安全的替代物
有三種類型的大腦替代物可以讓研究人員研究活人大腦的工作方式,它們可以避免手術的潛在風險——如果還不把它們視爲有違倫理。
人腦類器官。和其他模仿眼睛、腸道、肝臟、腎臟和其他人體組織的三維多細胞結構一樣,人腦類器官可以通過類似的方法生產出來。通過添加適當的信號因子,多能幹細胞聚合體可以分化和自組織成類似某些人類腦區的結構。
研究人員會使用不同的方法生產人腦類器官。他們可能誘導多能幹細胞轉化爲特定的神經細胞羣,例如特定腦區獨有的神經細胞羣。或者,他們也可能讓多能細胞自行分化,在這種情況下,它們既可能分化成神經細胞,也可能分化成其他類型的細胞。類似特定腦區的人腦類器官甚至可以被組合成“大腦組裝器官”,使研究人員能夠研究不同腦區之間的神經迴路和細胞相互作用是如何形成的。
與培養皿中神經細胞的 2D 薄片相比,3D 結構的壽命更長 (約爲兩年),並且可以含有更多不同類型的細胞。它們還能模仿一些大腦發育的關鍵特徵。例如,在胎兒發育的後期,大腦皮層從生成神經元逐漸轉向生成膠質細胞 (大腦中滋養、圍繞和保護神經元的各種其他細胞類型)。研究人員可以在人腦類器官中觀察到這一過程,否則如果要利用正在發育的真正人腦,在實驗難度和倫理上都極具挑戰性——如果算不上在倫理上絕對無法接受的話。
研究人員已經在利用人腦類器官來調查自閉症譜系障礙或是精神分裂症患者的神經發育異常,並研究在出生之前就感染寨卡病毒的部分嬰兒出現的小頭畸形。人腦類器官也有其侷限性。它們缺乏某些細胞類型,如小神經膠質細胞和形成血管的細胞。今天,最大的人腦類器官直徑大約 4 毫米,只含有 200 萬到 300 萬個細胞,而成年人的大腦的體積約有 1,350 立方厘米,由 860 億個神經元和數量相當的非神經元細胞組成。此外,到目前爲止,人腦類器官只能接收到形態最原始的感覺信號輸入,而來自其他腦區的神經連接較爲有限。
考慮到這些限制因素,人腦類器官在某種程度上變得有意識,或者獲得其他更高級的認知能力(比如感到痛苦的能力)的可能性似乎極小。但是,人腦類器官正在變得越來越複雜。事實上,本文作者之一 (Paola Arlotta) 在用光照射到人腦類器官上視網膜細胞與腦細胞一起形成的一個區域後,記錄到了來自人腦類器官的神經活動。這說明外部刺激可以讓人腦類器官產生反應。
體外腦組織。另一種類型的模型包括在某些手術過程 (例如癲癇手術) 中被切除的腦組織切片。

一個研究人員在解剖人類腦組織切片。
Credit: Darragh Mason Field/Barcroft Images/Getty
一個多世紀以來,研究人員一直在研究從接受手術的病人或已經死亡的病人身上提取的組織中的腦細胞。而技術的進步,包括成像技術和用於保存實驗室中腦組織功能特性的技術,可以使這種方法變得更加強大。
當大腦新皮層和海馬區的組織被切除以治療一些疾病 (比如癲癇或癌症) 時,取出的組織大小通常和一塊方糖差不多,大約 1 - 4 立方厘米,不過有時也會比這大很多。它通常會被切成薄片,這些薄片的功能特性可以保存數週之久。
研究人員可以利用這些切片,測量完整的大腦神經迴路中神經元的突觸和其他組成成分;繪製腦回路三維形態圖;提取和分析細胞 RNA,以探索基因表達。他們還可以利用光遺傳學技術來操縱特定神經元的激活,這可以使他們更詳細地分析人腦神經迴路的功能特性。(光遺傳學利用光來追蹤或選擇性地激活一些神經元,這些神經元已經經過基因改造,能夠表達一種光敏蛋白質。)
目前,體外腦組織沒有感覺信號輸入。由於體外腦組織的外向連接被切斷,這些孤立的組織無法與大腦的其他區域交流,也無法輸出運動信號。因此,體外腦組織出現意識或其他更高級感知能力的可能性看起來極小。
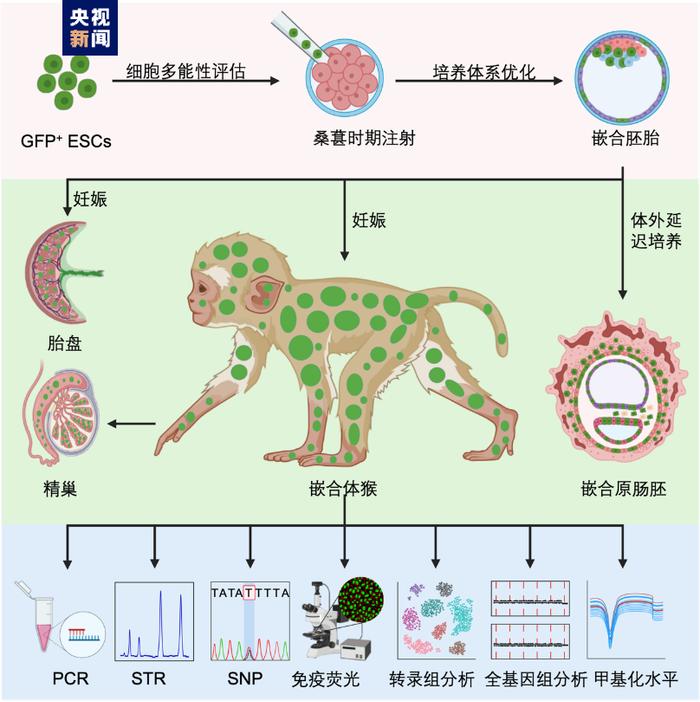
人獸嵌合體。第三類實驗大腦模型涉及到人類細胞的移植,這些細胞是在試管內由多能幹細胞體發育而來,隨後被移植進入其他動物的大腦,比如齧齒類動物。這個過程可以在動物胚胎髮育時,也可在動物出生後完成。這樣的嵌合體能夠提供一個從生理上而言更自然的環境,讓人類細胞在其中成熟。
舉例而言,神經科學家已經將人類的神經膠質細胞移植到小鼠身上,並發現移植後的小鼠在某些涉及學習的任務中表現得更好了。研究人員還曾將人類幹細胞注入到豬的早期胚胎中,然後將這些胚胎移植到代孕母豬體內,在那裏它們一直髮育到妊娠早期。這其中有超過 150 個胚胎髮育成了嵌合體;在這些胚胎內,心臟和肝臟的前體細胞中大約有萬分之一是人類細胞。
原則上,嵌合體可以幫助研究人員更好地瞭解人類疾病和藥物治療的效果。比如一些實驗室爲了研究帕金森病而培育了人 - 鼠嵌合體。
一些研究甚至已經成功地將人腦類器官移植到齧齒類動物中,在動物體內腦類器官得到了血管的支持 (血管化)。給人腦類器官供血是使其體積成長至超過目前可達最大體積的關鍵一步。但是齧齒類動物模型的大小限制了人腦類器官在其體內生長的程度。

源於幹細胞的 3D 人類大腦組裝體。
Credit: Pasca Lab/Stanford University
需要考慮的問題
目前,如果不在活人身上開展人體組織研究,那麼只有獲取、存儲、分享和識別組織的過程纔會受到具體規定和指導方針的限制,這些規定限制了人們對人體組織所能實施的干預的程度。隨着腦替代物變得更大且更復雜,它們擁有類似人類知覺的能力的可能性會變得沒有那麼微小。這種能力包括能夠感覺到(某種程度上)的快樂、疼痛或痛苦;能夠存儲和檢索記憶;或者甚至有一些對主體的感知乃至自我認知。
既然如此,利用從活人或屍體身上移除的腦組織開展研究,是否能夠提供關於此人記憶的信息?那些不是“生物學意義上的人類”的生物組織是否應具有一定程度的等同準人類乃至人類的倫理地位?
鑑於這種可能性的存在,我們在這裏列出了一些我們認爲公民社會、研究者、倫理學家、研究資助者和評審人應該加以考慮的問題。
測量指標。是否有可能評估一個大腦替代物的知覺能力?研究人員應該測量什麼?如果能開發出適當的指標,研究人員應當如何判斷大腦替代物的哪些能力在倫理層面上是令人擔憂的呢?
神經科學家在識別和意識相關的神經活動方面已經取得了相當大的進展。然而,在一個活的成人體內檢測到的有意識或者無意識的信號——比如使用腦電圖(EEG)電極獲得的信號——並不一定在嬰兒、動物或實驗大腦替代物中也成立。如果我們不能更進一步瞭解意識是什麼,以及它需要哪些基礎才能產生,就很難知道我們應當在一個實驗大腦模型中尋找什麼信號。
至於人獸嵌合體,研究人員本就已經在與具有某種意識的生命體打交道。因此,我們面臨的一個更緊迫的問題是確定以何爲基礎來採取保護措施,既是來保護人類研究對象,也是來保護動物研究對象。一種可能性是研究人員使用麻醉藥或其他方法來維持類似於昏迷的大腦狀態。又或許特定大腦功能或預先設定的大腦活動水平,能表明嵌合體缺乏對應的能力,從而證明研究的倫理合理性。
人與動物界限模糊。通過向小鼠胚胎注射大鼠多能幹細胞,研究人員已經培育出了長有大鼠胰腺的小鼠。利用同樣的方法,或許有一天也能使人體器官在其他動物體內生長。
我們如何定義這類研究的邊界?這樣的邊界對血管化腦類器官,或是在動物體內培育神經組織可能產生什麼影響?舉例而言,是否在豬的體內培育人類心臟就可以接受,但通過人類細胞培育大腦就不行?
我們認爲在決定哪些類型的嵌合體可被允許,或者判斷在動物身上培養的某些人體器官是否會使動物“太像人類”時,應該具體情況具體分析——風險、收益和人們多種多樣的敏感性都應當被考慮在內。
死亡。體外的人類大腦模型是否會挑戰我們對生與死的理解?這樣的替代物會給對死亡的法律定義帶來什麼影響?而對於與這一定義相關的決定,比如器官捐贈,這又會有什麼影響?
20 世紀 50 年代氣道正壓通氣的出現和 20 世紀 60 年代心肺復甦(CPR)的出現帶來了腦死亡的概念。從 20 世紀 60 年代開始,一個大腦完全不可逆地停止運轉的人,即使還有心跳,也可能被宣告死亡。
任何可能恢復大腦已喪失功能的新興技術都有可能導致腦死亡這一診斷的失效,因爲大腦功能的停止可能不再是永久性的和不可逆轉的。但是這裏需要做一個重要說明:只能恢復一些神經元或部分有限種類的腦活動的技術,並不會恢復大腦的臨牀功能,因此不會引起這種擔憂。
知情同意權。對於使用人類腦細胞或腦組織,或是使用通過誘導多能幹細胞培育的腦替代物的研究來說,獲得知情同意的通用標準流程是否就足夠了?
目前,使用多能幹細胞或腦組織的研究人員通常會向捐贈者大致公開他們的計劃。考慮到人們往往將他們的經驗和自我意識與他們的大腦聯繫在一起,研究人員有必要在這方面提供更多的透明度和保障。比如說,捐贈者們可能會拒絕使用自己的幹細胞來培育人獸嵌合體。
這種有針對性的獲取知情同意的方法已經應用在其他情況下了。比如,當接受體外受精治療的人選擇捐獻多餘的胚胎用於研究時,他們會得到研究人員的保證,保證這些胚胎不會被用來製造嬰兒。
監管工作。我們是否有必要擔心大腦替代物或嵌合體的福利,比如是否有必要給每一個大腦替代物分配一個有點兒類似於監護人或決策者的人——非參與研究的研究人員?這樣的安排類似於在美國的兒童監護權糾紛中,爲兒童指定一名監護人(父母之外可以代表孩子利益的一個人)。
所有權。誰應該“擁有”體外腦組織、人腦類器官或是嵌合體?真的有人應該有這個權力嗎?
目前,腦組織樣本由收集組織或從事科學研究的研究人員或組織擁有。如果有一天,這一領域的重大進展使我們認爲這些大腦替代物的倫理地位比我們目前所給予的要更高的話,是否有必要給它們更大的特權和保護呢?
研究後處理。在實驗結束後,我們應當如何處理或是安置人類的腦組織?
目前在研究結束後,人腦類器官或是體外腦組織會按照處理所有人體組織的標準流程被銷燬。但是,如果研究人員培育出了一些具有高級認知能力的小鼠,那麼在研究結束後,這些動物應該被銷燬還是給予特殊待遇?已經有一些動物,比如說黑猩猩,在研究人員在實驗室裏完成了研究工作之後,就會被放入保護區度過餘生。
數據。對於腦組織的數據共享、協作和遺留使用,是否應當有特殊要求?我們需要考慮一下分享從這些組織中所獲取的數據的獨特收益和風險。
體外的人腦組織可以暴露一些敏感信息,比如一個人的記憶,或是其疾病狀況。同樣的,因爲獲得人腦組織十分困難,共享這類信息可能能帶來更多的價值。在某些情況下,可能需要剔除掉這些數據的某些特徵,或限制其共享的範圍。
長期以來,遺傳學家在測量人類基因組信息時一直面臨着類似的問題;他們的一些方法或可以被應用於大腦研究。
解決倫理問題
爲了解決神經科學進展所帶來的倫理問題,人們已經在做出各種努力。2013 年,當“腦計劃”對外公佈時,美國生物倫理問題研究總統諮詢委員會 (the Presidential Commission for the Study of Bioethical Issues) 肩負起了評估其倫理問題的任務,並發表了一份兩卷的報告。歐洲委員會的人類大腦計劃 (The European Commission’s Human Brain Project ) 有一個重要的倫理部門,而美國國立衛生研究院 (NIH) 的腦計劃 (BRAIN Initiative) 也有一個神經倫理部門。
但我們認爲還有很多事情要做。現有的機構倫理審查委員會或是幹細胞研究監管機構可能還沒有準備好解決這些實驗性腦模型所特有的問題,因爲這些問題都是全新的。我們建議這些組織邀請本領域的專家加入他們的委員會或是擔任顧問。此外,也應當組建專門負責監管人類大腦替代物使用情況的新委員會。
至於更廣泛的社會溝通,可以運用各種已經存在的進行民主審議的模式。一個例子是,公衆、科學家、監管機構和生物倫理學家順利地進行探討協商後,促使英國政府在 2015 年決定允許臨牀使用線粒體 DNA 轉移技術。
隨着這些對話的展開,生物醫學研究的主要資助者應該努力提供引導,並最終形成書面指導準則。此外,開發和使用人類大腦替代物的研究人員也應該自行尋求倫理指導,這些指導可以來自他們的資助人、審查委員會或是研究機構等。作爲評審人,他們也應該在自己的論文或會議上分享他們在這方面的經驗和擔憂。
我們不認爲我們應該因爲這些難題而停止這方面的研究。人腦的實驗模型可以幫助我們解開長期以來一直難以捉摸的精神病學和神經系統疾病方面的謎團。但是從長遠來看,爲了確保這方面的研究能夠成功且被社會接受,在大腦替代物研究仍處在初期階段的當下,我們必須建立起一個倫理框架。