第3代肺癌靶向藥!FDA批准輝瑞新藥治療轉移性肺癌
原標題:第3代肺癌靶向藥!FDA批准輝瑞新藥治療轉移性肺癌
近日,美國FDA批准了輝瑞該公司的第三代ALK酪氨酸激酶抑制劑(TKI)Lorbrena(lorlatinib)上市,用於治療ALK陽性轉移性非小細胞肺癌(NSCLC)患者。這些患者在接受crizotinib或者至少一種其它ALK抑制劑治療後疾病繼續惡化,或者接受alectinib或ceritinib作爲第一種ALK抑制劑療法後疾病繼續惡化。
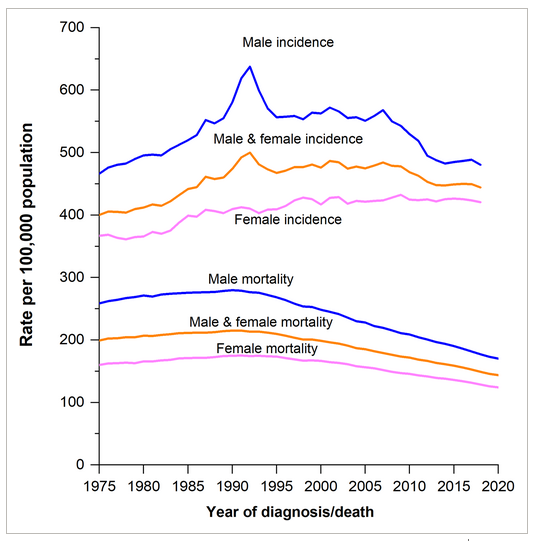
肺癌是世界上導致癌症死亡的首要原因之一。每年死於肺癌的患者超過死於結腸癌,乳腺癌和前列腺癌的患者總和。肺癌主要分爲小細胞肺癌和NSCLC兩種,NSCLC是最常見的肺癌種類,大約佔肺癌患者總數的85%。雖然很多ALK陽性轉移性NSCLC患者對最初的TKI療法產生響應,但是他們的腫瘤通常會再度惡化。而且,對於那些接受過第二代ALK TKI治療,但是疾病繼續惡化的患者來說,他們的治療選擇非常有限。
Lorbrena是在臨牀前肺癌模型試驗中對攜帶ALK和ROS1染色體重組的腫瘤表現出很高活性,能夠抑制對其它ALK抑制劑產生抗性的腫瘤突變,並且可以穿過血腦屏障。此次批准是基於一項B7461001的實驗,評估了Lorbrena治療既往接受過一種或多種ALK-TKI治療後病情進展的ALK陽性轉移性NSCLC患者的療效和安全性。研究共入組了251例患者,結果顯示,Lorbrena治療的總緩解率爲48%;重要的是,在既往接受過2種及更多種ALK-TKI的亞組患者中,Lorbrena的總緩解率提高到了57%。該研究中,有69%的患者存在腦轉移,這類患者中Lorbrena的顱內緩解率爲60%。
該藥物已獲得FDA授予的突破性療法認定,且獲得了優先審評資格。目前,Lorbrena也已獲日本批准,用於對ALK-TKI耐藥或不耐受的ALK融合基因陽性不可切除性晚期和/或複發性NSCNC患者。(楊麗萍/編譯)
資料來源:
①輝瑞官網:U.S. FDA APPROVES LORBRENA® (LORLATINIB) FOR PREVIOUSLY-TREATED ALK-POSITIVE METASTATIC NSCLC
(責任編輯:楊麗萍)
查看原文 >>