抗擊疫情:如何在實驗室檢測新型冠狀病毒?
出品:新浪科技《科學大家》、未來論壇
主講嘉賓:黃岩誼 北京大學化學學院教授,北京未來基因診斷高精尖創新中心研究員、副主任,北京大學生物醫學前沿創新中心研究員,北京大學—清華大學生命科學聯合中心研究員

這是2019年12月31日新年鐘聲敲響之前的兩小時,我在北大拍的照片。湖面結了冰,未名湖上的反光,是博雅塔上亮着的燈。那一天我比較忙,沒有看新聞消息,後來才知道在武漢出現了不明原因的肺炎。隨後幾天我們得到很多新聞消息的推送,我也開始關心這個消息,雖然我當時並不知道這個突發的情況會不會影響到我的生活。
大概一週時間之後,肺炎元兇已經確定了,這時候我開始關注它了。爲什麼呢?因爲這是一個新型冠狀病毒,雖然我不懂冠狀病毒是什麼,但是這裏說得到了該病毒的全基因組序列,這個我就有興趣了,因爲我是做測序研究的科研工作者。當我看到從序列來確定病毒的時候,我想這真是很了不起的。從我看到這個新聞,到得到最終結果纔過去不到一星期的時間,這是非常難以想象的快速度,僅僅只用了幾天時間,我們就確定了新的病原體。
如果是一個新傳染病,該怎麼做呢?這從來都不是一件容易的事情。一開始網上傳的消息說是SARS,也是我們常說的非典,再次歸來。這次能夠這麼快的發現它不是SARS,而是個全新的病毒,還跟SARS很接近,得益於過去十五年左右的時間內,高通量DNA測序技術的飛速發展。
通常鑑定一個疾病的病原,要符合所謂的科赫法則。也就是說,首先要找到宿主體內的致病微生物,發現它不存在於健康生物體內;要想辦法分離出來,得到它的純培養物,重新接種到宿主體內,再次分離得到這個培養物,發現這個培養物接種的宿主必定會導致疾病的發生,等等。
科赫法則是在130年前正式發表的,到現在爲止還主導着絕大多數傳染病病原體的診斷標準。只不過隨着科技的發展,在新時代到來的時候,隨着基因組學的快速發展,很多法則用到了新的病原體鑑定的時候,有了新的變化。
舉個例子,比如說肺炎,它的症狀,通常是患者肺泡內充滿液體出現氧合不良。肺炎是什麼病原體導致的呢?可以說有很多。除了最常見肺炎鏈球菌之外,還有很多病原體可以引起肺炎。比如說這些下圖所示的各種病原體,我從網上查來的,都有可能引起肺炎。
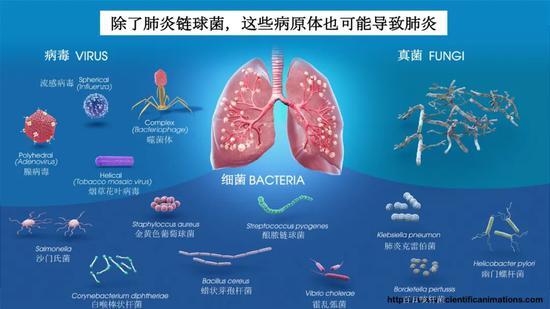
總的來說,分成病毒、細菌和少數真菌這三大類。病毒是裏面最麻煩的,因爲它特別的小。病毒跟人類相伴了很長的時間,人類文明史上從來沒有間斷過,一直有它的存在,很難對付。病毒在地球上待的時間比我們長多了,隨着人類文明的一步一步發展,它永遠跟着我們走。現在由於疫苗的大量普及而慢慢少見的脊髓灰質炎,也就是小兒麻痹症,也是花了半個多世紀的時間才基本根除。幾個月前看到世界衛生組織的新聞,宣佈在世界範圍內消滅脊髓灰質炎Ⅲ型野病毒,這是一個亞型被完全消滅。
病毒難以對付的一個原因,是它特別小,它的尺度和肉眼所及的尺度是很不相配的;肉眼是看不到病毒的,數量級相差太多了。光學顯微鏡出現之後大大幫助了生物學家和病理學家找病原體,它幫助科赫確定了結核桿菌、霍亂弧菌這些病原體,但是他沒有辦法用這些工具來發現病毒這個病原體,這超出了光學顯微鏡的極限。
直到1939年到1940年間,德國科學家Ruska第一次在電子顯微鏡下看到了病毒顆粒,有菸草花葉病毒、牛痘病毒等。這不得不感謝大他兩歲的哥哥,他哥哥是電子顯微鏡的發明人,後來晚年得了諾貝爾獎。這次我們對新冠病毒的確定,也多虧了這些新技術的發展。
科學論文助力人類全面瞭解新冠病毒
讓我們回到今年一月份。一月下旬,幾篇中國科學家撰寫的科學論文相繼面世,使得我們可以全面瞭解這一個新的病原體。新聞報道,只是新聞,但是讀科學論文,可以感受到細節的重要性。首先,1月24日的《新英格蘭醫學雜誌》上,我們看到了這個病毒的全基因組序列。從序列上,生物學家可以很明確地判斷這是冠狀病毒,而且從序列分析上可以判定這是一個新病毒,在人類歷史上以前沒有發現過的新病毒,歸屬到Beta屬,是感染人類的冠狀病毒科的第七個成員。
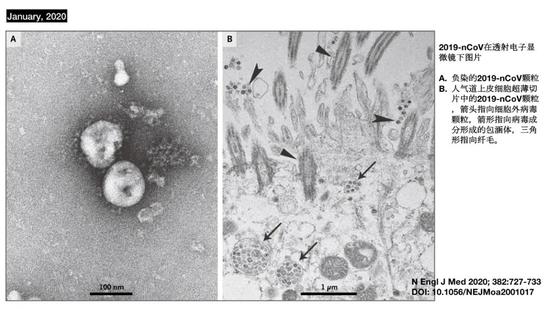
上圖是第一次科學論文中展示新冠病毒的透射電子顯微鏡照片,可以看到它個頭很小——對照比例尺,它的大小隻有100nm左右,但是長相和其他冠狀病毒非常相似。
同一天,《柳葉刀》雜誌上發表了由中國醫科院病原所王健偉教授和中日友好醫院曹彬主任的團隊對新冠患者的臨牀特徵的研究結果。這裏第一次提到對病人確診的時候使用了一個技術,即RT-PCR方法,來進行核酸檢測。種種跡象表明這是一種新疾病,給我們帶來了新挑戰;不僅給科學帶來了新挑戰、給醫學帶來新挑戰,也給病人帶來新挑戰。
第三篇重要的論文,是在我們中國自己的期刊《中華醫學雜誌》上發表的,這篇文章很系統地描述了新冠病毒的特徵。在隨後在中國科學報的新聞中,可以看到這個病原鎖定的過程,非常地迅速、高效。幾個團隊平行行動,開始進行測序,使得結果的可靠性大大增加。在血清學的研究中,還揭示了病毒與患者恢復期的血清之間的抗原抗體反應,這是一篇很完整的科學論述。
第四篇,是這三個平行檢測中的另一個團隊,武漢病毒所的團隊。他們的結果,和之前其它團隊的一樣,得到了幾個病毒的全序列。
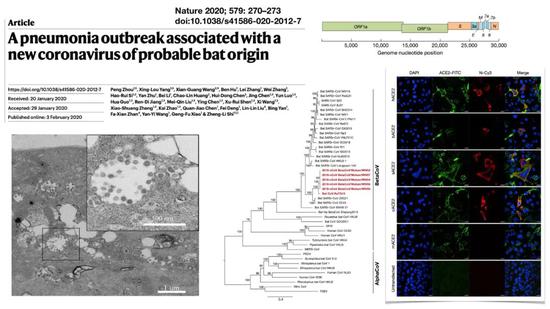
另外一個重要結果是右邊這些彩色的光學顯微鏡展示(上圖)人的ACE2蛋白是病毒侵犯人體細胞的重要途徑,這對於病毒致病機制研究和治療以及藥物開發都提供了重要的線索。
第五篇論文是和上一篇同時發表的,上海團隊,從早期武漢一個單個病人身上獲得樣本,通過高通量測序方法,得到了病毒的全序列,拿它和SARS病毒的序列作了比較。正是由於中國科學家們在1月份第一週之內快速響應和高質量的工作,很快病毒的參考基因組得到了。通過參考基因組,我們就有了座標系。
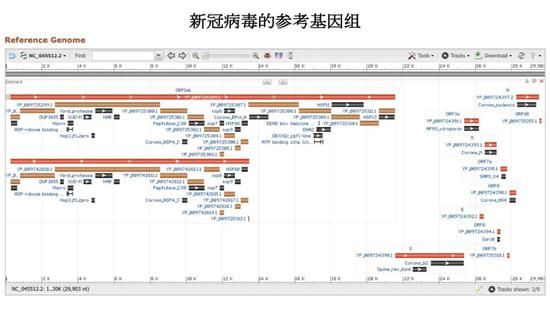
首先,可以理解病毒基因組的每一段序列是幹什麼。比如上圖標記出來得“道道”,就是一個個基因,用來編碼一段一段有功能得蛋白,行使特定的功能,有的是讓病毒可以複製,有的是讓病毒有利於侵入人體,有的是構建病毒的結構框架。其次,有了這個參考座標,以後病毒再發生了變異,我們就知道什麼地方發生了什麼變異,這對我們更深度的理解病毒生物學的基本功能,以及它的自然史,以及疾病發生與發展有非常重要的意義。
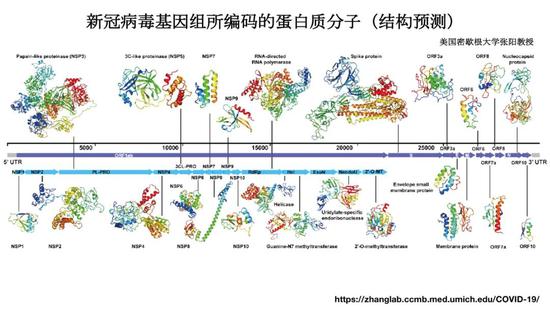
上圖是病毒基因組編碼的主要蛋白質,展示的是預測的蛋白質結構,是美國密歇根大學張陽教授團隊的結果。從這裏可以看到,這有個很重要的蛋白,叫做Spike protein(S蛋白),還有別的比如M蛋白、N蛋白等等,這些不同的蛋白是這個病毒中非常特異表達的蛋白質。通過這些結果可以構建出來,現在經常可以在新聞中看到的新冠病毒的模型圖,病毒外表上這些蛋白一般就是我指的這些蛋白,這些蛋白給病毒特定的功能,不僅給它一個結構支撐,而且對我們做檢測來說也能成爲我們重要的目標。我們可以通過檢測這些病毒的特定成分例如目標蛋白或者編碼這些蛋白的基因來確定病毒的存在。
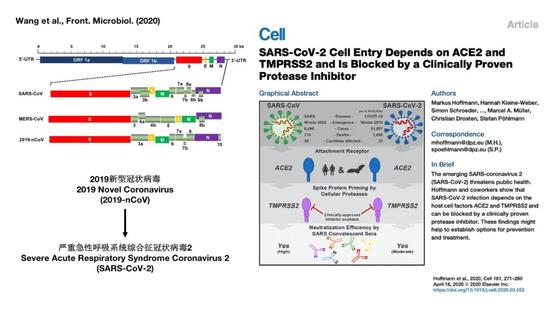
正是由於我們對於病毒的序列的解讀,我們馬上就可以知道它和17年前的宿敵SARS冠狀病毒是近親。都不需要告訴大家怎麼看這個圖,可以看出它們是蠻像的。它不僅和SARS很像,和10年前的MERS也有關係。這也說明了我們不能小瞧這個病毒,它可能具有巨大的破壞力。由於與SARS的相似性,國際病毒命名委員會,將原來我們把它叫做2019新型冠狀病毒改名嚴重急性呼吸系統綜合症冠狀病毒2即SARS-CoV-2。SARS-CoV-2表明它跟原來SARS病毒之間的關聯性還是比較近的。前不久德國科學家的論文也說明這個新的SARS冠狀病毒和原先的SARS病毒確實在攻擊細胞的時候採用的策略極爲相似,通過進攻同樣的蛋白來侵入細胞。而且還發現之前SARS病毒的抗體對新病毒也具有一定的中和作用,揭示兩種病毒的高度相關性。
進入生物分子學的時代,對於傳染病的認識開始變化,都從分子水平理解開始。知道了冠狀病毒,就不像2003年那樣,那時我們一開始還不能確定病原體,叫它非典型性肺炎。現在國際衛生組織命名這個新的疾病爲“2019冠狀病毒病(COVID-19)”,即由冠狀病毒感染引起的疾病,而不是用簡單症狀來命名。我們國家衛健委的命名還是“新型冠狀病毒肺炎”。所以大部分時候我們在中國,還是用新冠肺炎來稱呼COVID-19。
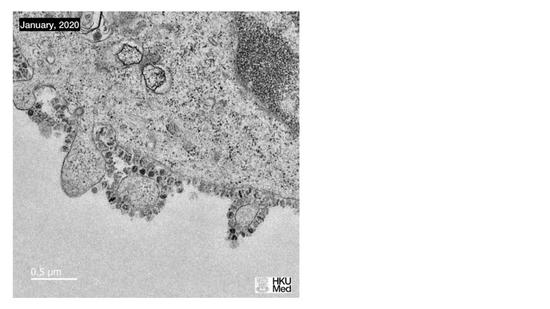
上圖是香港大學的科學家1月份看到的冠狀病毒,這個病毒已經完成了複製,從細胞裏面釋放出來。
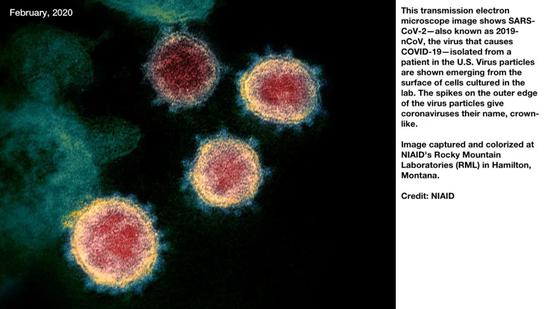
上圖是2月份美國科學家拍攝的冠狀病毒的大頭照,可以清晰的看到表面“花冠的出現”,這是一個僞彩照片,很好的標出了“花冠”的存在。
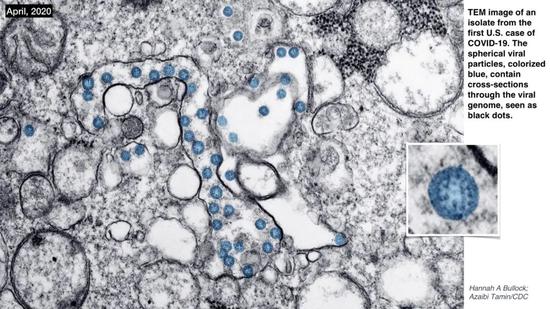
前不久美國疾控中心發佈新的冠狀病毒的集體照(如上圖),藍色標出來的是病毒顆粒,病毒顆粒裏的小黑點就是切開了的斷面上的核酸,就是這些冠狀病毒裏包含了基因組的部分。這個基因組對於我們做檢測有極其重要的意義,是我們檢測的物質基礎。
疾病診斷重要組成部分:分子診斷
分子診斷對於疾病診斷來說是重要的組成部分,疾病診斷是複雜問題,尤其是新疾病出現的時候,對於一個傳染病來說,已知病原體的情況下分子診斷成爲極爲重要的指標。
它的主要目的有以下幾個:第一,它確定臨牀症狀,比如發燒是否是由新冠病毒引起的,避免它和其他疾病混淆起來。第二,對疾病的進程進行定性(比如陽性陰性)或者定量描述,比如病毒載量的多少。第三,從更加精細的角度出發,某些分子診斷還可以提供疾病的治療方案,幫助確定它的方案,提供證據的支撐。第四,從病毒疾病的角度出發,可以追蹤變異情況,這也非常重要,研究並且預測病毒在傳播過程中的傳染和致病能力的演化,比如我的同事北京大學陸劍老師的文章,他指出有一些關聯性特別密切的突變位點,很可能和疾病的愈後之間有着非常緊密的指徵性連接,所以很可能對以後疾病的救治,以及理解病毒怎麼跟宿主共同生存有很重要的意義。
什麼是分子診斷?狹義的分子診斷一般來說就是核酸檢測,包括對特定核酸片段的定性和定量分析,利用核酸雜交芯片、測序技術等等做序列分析。如果要拓展成廣義的分子診斷,也許還可以涵蓋其它和傳統病理診斷相對應的分子病理技術包括抗體檢測等。不過約定俗成,一般情況下我們說分子診斷就是說核酸檢測。核酸檢測是指檢驗樣品中間是否含有特定序列的DNA或者RNA的片段,作爲病原微生物存在的證據。除了病原微生物的分子診斷外,這一方法在疫情之前就已經被用的很普遍了,比如說大量的其他感染性疾病的診斷、遺傳疾病的診斷、腫瘤的分型、化療用藥的指導等很多醫療實踐中都用到核酸,只不過那時候沒有像今天提的這麼多而已。

除此之外我們針對抗體做檢測就是抗體檢測,抗體檢測看的不是病毒本身,而是看血液中間或者體液中間有沒有抗體分子的出現。
還有一種檢測是抗原檢測,目標是病毒身上的物質,比如我們上圖中看到的藍色標記的這兩個地方,這兩個都是病毒獨有的蛋白,刺突S蛋白和核衣殼N蛋白,看他們是否存在於樣品中,就是抗原檢測。這都是基於我們要檢測的時候的物質基礎。

檢測,歸根到底是針對分子的測量,測量分子數量的多少;這是由病毒本身的結構和組成來決定的,都有其物質基礎。這幾位以色列和美國的科學家,把冠狀病毒的一些關鍵數據列了出來。從檢測上講,除了核酸分子(上圖中綠色箭頭標出來的),它是每個病毒裏有一條分子外,還有很多蛋白質分子(幾個紅色箭頭標出來的),在病毒裏數量很多。但是這些分子的數目分佈還是有區別的,S蛋白,大概每個病毒有上百個;N蛋白和M蛋白每個病毒有上千個。對這些數量的瞭解非常有助於我們今後發展特異性的檢測技術來確定病毒的存在。
從新冠病毒肺炎的第七版診療方案中可以看到,診斷指標列的非常明確,在病原體上的證據有兩項,一是熒光RT-PCR,二是基因測序。病毒的核酸序列特徵和其他物種比如動物和人的核酸序列大不相同,通過這兩個方法可以對序列鑑別不太容易出錯。隨着疫情的發展以及我們對病毒自然史認識的加深,診療方案調整到後期的時候,把血清學檢測也加上了,我們以後再講。
核酸檢測 Vs 抗體檢測
關於檢測,國家衛健委的通報和藥監局的審批一直都是圍繞核酸和抗體進行。這兩個檢測方法完全不一樣,目的不同,採的樣品來源不同,檢測方法不同,結果解讀不一樣,適用範圍也不同。下面稍微介紹一下這兩個方法。
核酸檢測,首先是採樣。

現在接受核酸檢測的人多了,大家看的新聞也多了,看到上圖這樣的圖片不會覺得太新鮮了。事實上我自己去年以前沒有體驗過咽拭子是怎麼回事兒。更多人只是在圖片上看到過這樣的實驗室環境,並沒有真正的體會過。真實過程比圖片展示的可能還要複雜一些。採樣,一般都在實驗室外相對空曠的地方,採樣人員必須經過專業培訓,還要注意防護。因爲這是有風險的操作,不僅僅面對有可能帶傳染能力的感染者,還包括採樣過程中本身會增加暴露的風險。比如採樣中打個噴嚏或者咳嗽,都會增加暴露風險。
要確保採樣成功有兩個關鍵,一個是使用的材料即拭子是有講究的,不是隨便一個棉籤就可以;同時,拭子採樣後的保存環境也是有講究的。另外採樣本身的操作是有講究的,手法也重要,也不能過去一捅就能夠採到。採樣的部位選擇和操作都是獲取高質量樣本的基礎,只有樣本質量好,纔有可能做出可靠的檢測。
舉個例子,最常見的樣品就是鼻咽拭子,注意採樣的拭子要一直伸到鼻咽部的最後面,在口咽部的上方。這不是一個很容易的操作,很講究經驗和手法,自己做也是有困難的,一般也不推薦自己這麼採樣。還有喉咽拭子,張開嘴,也是要將很長的拭子深入到口腔後部,在咽喉部位,扁桃體邊上。這個取樣也不是自己可以簡單做的,通常還要把舌頭壓下去。爲什麼採樣這樣講究?因爲採沒采到、採沒采好,直接決定了你做的檢測到底能不能看到可靠的結果。
採樣部位的不同反映在檢測結果上也不一樣,中國科學家們很早就總結了一些規律。

比如,從上圖a,看得出來隨着症狀的進展,慢慢的好像信號就下去了。隨着(出現症狀之後)時間增加,採樣得到的核酸數量越來越少。另一個結果,從c圖上可以看到鼻咽拭子採到的核酸量會比喉咽拭子高一些,穩定性也稍微好一些。早期得到的經驗對後面指導採樣的流程有重要的意義,就是應該怎麼採、採什麼地方的樣品。
疾病的特點導致了病毒侵染部位有特點,既有偏好,也受發病時間的影響。實際上,作爲檢測,可以用各種樣品,不僅僅只是兩種拭子。第七版的診療方案中明確提出了鼻咽拭子、痰、其他下呼吸道分泌物、血液、糞便的標本中都可以測出病毒核酸。還有調查研究表明,這麼多的論文總結起來,看上去在很多樣品中比如眼淚、糞便中都可能檢測到核酸病毒,但這裏面痰液或下呼吸道分泌物是最不容易漏檢的,也就是檢出率是最高的,接下來就是鼻咽拭子。所以可以發現真正做高質量的測量研究中,對樣品的來源非常考究,要求一定要保證樣品採樣的質量,只有拿到好的樣品纔可能得到好結果。世界衛生組織在1月份就有指導文件,對不同樣品的採集、保存、用途都做了很好的梳理,有了這樣的指南,世界各地的科研人員和醫務人員都可以遵循相對正規可靠的流程,來保證結果的可靠性。
樣品採集後做檢測,第一步通常是核酸提取,就是把樣品中的核酸部分留下,其他部分雜質、人脫落的細胞、其他分子如蛋白質分子等等都除掉。通常的核酸提取,採用的都是把核酸分子用和它親和力強的材料,例如硅膠等,先吸附;等到把其它物質都分離掉後,在把吸附的核酸分子洗脫下來,實現了提取,同時也是純化和富集的步驟。這裏可以採用的,在實驗室裏面,有兩個方法。這兩個方法現在在新冠病毒的核酸檢測中,都廣泛使用。要麼使用硅膠膜來吸附,要麼利用表面修飾的磁性小顆粒來實現吸附。這個步驟看上去很簡單,但是這裏最關鍵的一點,是要考慮到生物安全。
有興趣的觀衆,可以看中國醫學科學院北京協和醫院的培訓教學視頻,這個視頻完整的演示了怎麼做核酸提取,也強調了操作人員的生物安全問題。爲了保證這一點,特別指出所有樣品在操作前要先置於56度的水浴箱裏進行30分鐘滅活,使病毒失去感染能力。國家衛健委發佈的《新型冠狀病毒實驗室生物安全指南》也說,未經培養的感染性材料的操作需要這麼做,應當保持在生物安全二級標準的實驗室進行,同時採用生物安全三級實驗室的個人防護。
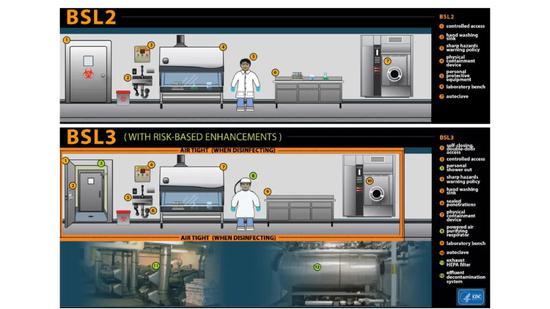
上圖美國CDC的卡通圖。生物安全三級,簡單說是在封閉空間在採用負壓,所有的空氣跟其他物質不會沒有經過處理直接外排到外界,這樣一個生物實驗環境。裏面的人員和我們常在電視裏看到的全副武裝的白衣戰士差別不大,都是一樣的裝束,只會更加嚴格,需要完全沒有暴露的身體部位。生物二級要求沒有那麼嚴格,空氣和外界有交換,有時在個別區域可以增加生物安全等級,做要求更高的實驗。這次吳晨老師帶領的武漢的方艙檢測國家隊,就是在一個移動的生物安全三級實驗室工作的。

上圖是吳晨教授在武漢現場工作的照片。左邊的工作環境是生物安全二級,右邊那個車是移動的生物安全三級的實驗室,吳晨老師的打扮是標準的生物安全三級的打扮,如果不是有名字寫在那裏,其實你並不知道她是誰。全副武裝做實驗,是出於生物安全的考慮。

核酸提取之後是擴增的步驟,這是通過廠家提供的幾管試劑實現的。上圖中左邊是華大基因的試劑,裏面是幾個小試管,右邊是美國疾控中心分發的試劑,裏面也是幾個小試管。檢測的過程叫做RT-PCR,就是逆轉錄-聚合酶鏈式反應。這是一個利用自然中存在的核酸複製機制來實現DNA分子的體外複製的操作,已經發明瞭近四十年,是分子診斷的基礎技術,也是現代生物學和醫學進步的重要奠基性技術。在每一個試管中,除了加待測樣品就是核酸提取液外,還要加DNA聚合酶,逆轉錄酶,以及引物和探針。新冠病毒是RNA病毒,病毒裏面包裹這一條基因組RNA,通過逆轉錄酶把這條RNA變成和它互補的DNA,然後再複製一遍,變成雙鏈DNA,再往後就可以通過熱循環一遍一遍的解開配對的雙鏈,分別複製。1變2、2變4、4變8,經過N輪循環,理論上可以得到幾何級數增長的特定片斷的DNA。在複製的過程中,一個巧妙設計使每一次的複製能產生特定的熒光分子,複製的分子越多產生的熒光越多,我們就可以檢測到這信號,這樣一輪一輪的複製下去,我們看熒光增長。如果有熒光增長就是有待測物質,即所謂陽性;沒有增長就是沒有待測物質即所謂的陰性。熒光增長越快,就說明分子越多,增長越慢,說明分子越少,大概就這樣一個過程。
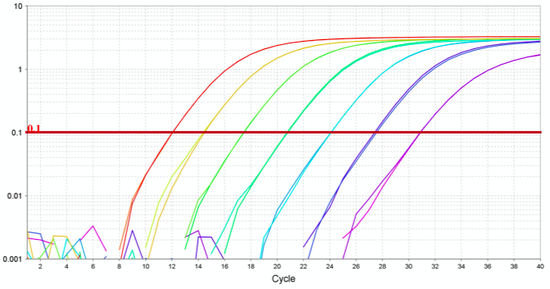
這個過程歷時不太長時間,能夠給出這樣一個圖來(如上圖),劃一條線切過去,與熒光強度曲線交叉得到的值如果是低的證明你可能是陽性,這個值太高了或者沒有出現(上升)證明是陰性。
這個判斷在實際上還是有講究的,做的過程中一定要加質控品,陰性質控和陽性質控都要有。一般來說陰性的就是純淨的水,裏面不應該有待測的核酸,不應該出信號;如果出了信號,這次實驗的可靠性就有問題。陽性的,一般是一個低濃度的樣品,如果我們沒有測出信號,證明這次實驗不夠靈敏,也許哪裏有問題了,需要檢查和重做。
另外,選擇探針序列也就是引物序列非常講究,在大概3萬個鹼基左右長度的序列,檢測哪一段還是需要下一番功夫的。一組韓國科學家,前不久發表了一個對比結果,把一月份就分別採用的核酸檢測的檢測位點,的有效性做了一個相對客觀的比較。各國科學家確定的用來做診斷的位點,是有區別的。上面這裏,我標出了這些檢測的核酸片段在基因組中的位置,比如中國的兩個位點,一個是ORF1ab,另一個是N;而美國的三個,都在N蛋白基因上;德國的,一個在RdRp基因上,一個在E基因上。

上圖是N基因的一段序列,裏面用顏色表示的是,各個國家檢測的位點,所使用引物的位置。可以看出,少量位置,各個國家的科學家們確定的有一些小的重疊,但是總的來說,並不是精確在一起。結果很有意思,韓國科學家的對比實驗提出來中國和美國選擇的位點是這些檢測中靈敏度最高的,這也從側面反映了我們科學家早期選擇位點的時候選的很準,這是需要經驗的,需要能力,也需要做出科學判斷的。
核酸檢測是否還可以改進?首先看速度,一個標準的核酸檢測過程,取樣是很快的,然後把它存到運送培養基裏,把樣品攢到一定數量的時候,集中滅活,56度、30分鐘,然後進行核酸提取;核酸提取差不多30-90分鐘,PCR反應40-60分鐘,這個是可以一批樣品,常常96個一起做的,出來之後可以快速結果判定,整個實驗做下來大概小半天的樣子。這個過程能不能加速?如果是單個樣品,樣品採集之後直接就做,可以跳過很多步驟,比如直接放到裂解液裏面,然後做快速的核酸提取,甚至不做提取就做快速的PCR,這樣可能在30分鐘左右就拿到結果。可以看到,PCR檢測本身是可以做到快速的,尤其是樣品量少的時候可以這麼做,但樣品多的時候最好是一批一批地操作更有效率。
我後面還會講到一些檢測方法,我們先看一下前幾天美國科學家的一個綜述,把最近報道的各種核酸檢測方法做了一個總結。
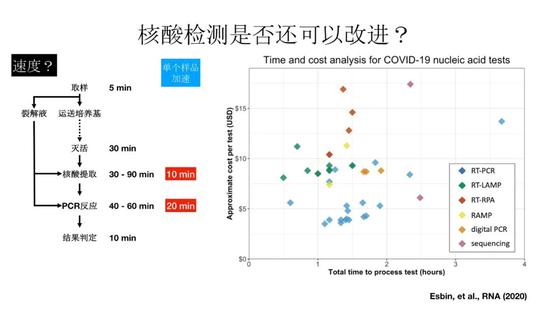
上圖可以看到,各種方法檢測所需的時間,大部分在一兩個小時內都能做完,價格從幾美元到十幾美元。這裏方法很多,有的已經不再是所謂RT-PCR方法,但還是充分借用了大自然的力量,利用自然界遺傳物質的複製機制,進行特定的DNA片段的擴增,最終達到足夠強的信號獲取。擴增反應本身可以通過各種巧妙的方法加以實現。除了RT-PCR這一被反覆驗證和優化了20多年,被證明爲極爲可靠的臨牀檢驗方法之外,還有很多其他擴增方法被髮明出來,面對新冠病毒的檢測這些方法正在經受嚴格的考驗。基於對檢測速度的追求,即使是通過RT-PCR方法,爲了減少操作上的技術壁壘和失誤,可以採用所謂POCT的設備,也就是可以在現場使用的小型儀器裝置。

上圖中的兩個是3月下旬的時候美國藥監局最早批准緊急使用的兩個儀器,分別可以在30分鐘或45分鐘內完成從樣品到結果的檢測全流程。在傳染病流行期間利用這樣的設備至少有兩個重要好處,一個是分散處理病人檢測需求,避免樣品積壓和運送困難。二是可以採用幾乎全封閉的實驗室設計,減少了操作者的生物安全風險。

上圖的儀器可能是這一類檢測儀器中最出風頭的,這是美國超級銷售特朗普親自帶貨的小儀器,很可惜他沒有擺對,圖中不是正確的擺放方法。這個機器可以在5分鐘之內給出陽性結果,十幾分鍾給出陰性結果,真正使用的時候整體所花的時間實際上會再長一些。要說明的是,這不是一個新的發明,不是有了新冠病毒突然就冒出了這麼一個新發明。這個儀器已經在市面上很長時間了,在被新東家雅培買走之前,它已經是市場上用來檢測流感病毒微生物的便攜設備。

比如上圖,這篇2014年深圳福田醫院的科研人員參與的一篇論文,就是在評價這個儀器檢測流感的表現。這個儀器用的基本技術是一個相對冷門的擴增方法,叫做NEAR(切口酶擴增反應),自然界存在很多奇奇怪怪的酶,可以做很多事情。切口酶就是在DNA切面上形成一個小切口,然後讓聚合酶找到那個地方,可以開始做複製,不斷的形成切口,不斷的複製。
這是非常巧妙的一個方法,不需要做PCR反應和熱循環,屬於等溫擴增的一種。等溫擴增的意思,是不需要做熱循環,擴增過程在一個恆定的溫度下進行,好處是這個過程變得非常簡單;另一個好處是快,因爲等溫擴增的檢測常常都是幾分鐘、十幾分鐘的時間尺度下完成的。
除了NEAR之外,還有很多等溫擴增反應可以利用在覈酸的檢測上。例如一個相對比較有名的LAMP環介導等溫擴增,這是日本科學家Notomi等人在2000年左右發明的,這個方法也是用四個或者六個引物序列加到待測物質裏面,把它的溫度稍微升一點,通常會在60度左右的溫度下做等溫擴增反應,不需要很複雜的儀器很快就能做完。
這個方法的一個好處是,設備可以做的很簡單,可以很容易操作,肉眼就可以做判別。中國藥監局也批准了基於這類反應的體外診斷試劑,例如這是成都博奧晶芯做的基於LAMP擴增方式的新冠病毒診斷設備。
還有其他方法,其中一個方法是RPA,也是相對比較容易。它用兩種酶的組合,重組酶和聚合酶放在一起,通過一個很複雜的循環,實現核酸分子的擴增,雖然複雜但是非常高效,非常快。基於RPA,在美國波士頓有名的華裔青年科學家張鋒,把它和基因編輯結合在一起,嫁接起來實現了對RNA的檢測,他們起了一個名字叫SHERLOCK(福爾摩斯的大名)還用這個名字註冊了企業,來做這個試劑的開發。無獨有偶,在美國加州舊金山,基於LAMP方法,嫁接基因編輯,Jennifer Donna跟她的合作者一起也做了一個新方法,叫做DETECTR,成立的公司叫做Mammoth Biosciences。這兩個方法比較上看,它們大概都可以實現30分鐘到50分鐘的檢測,相對都是快的。這兩個方法可以用試紙條的形式來讀取結果,也很容易被大家所領會,不需要複雜儀器。
除了縮短時間,對於大規模的檢測,提高檢測通量是非常重要的,試劑盒可以拿來一盒就可以做好多檢測,但是樣品要一個一個測。還有核酸提取這樣原來特別消耗體力而且需要經驗、技巧、訓練的工作,最好交給不知疲倦、不容易犯錯的機器來操作。所以我們看到核酸提取自動化儀器大量出現在檢測現場,這樣的儀器遍佈在各個定點醫院,各級的疾控中心。

上圖右邊這兩個儀器是在美國的大學實驗室內,現在大學實驗室大量加入到大規模檢測的隊列中來,能夠消除一些檢測滯後的焦慮。如果是一個集中處理的大型檢測結構,就要用更加完整的自動化的儀器纔好用。

上圖是羅氏公司做的巨無霸儀器,Cobas8800,一臺這樣的機器,一天不停機大概可以完成3000個核酸檢測,而且幾乎全自動,把樣品放進去之後就開始做。這有什麼好處呢?除了快之外,還有一個重要的好處是可以保證在世界上不同地點,大家取得的結果都是基本可靠和穩定的。這樣,在基礎比較薄弱、積累不夠雄厚的地方,一樣可以實現高品質的大規模檢測。在肯尼亞、在加拿大、在美國、在中國,得到檢測結果不會由於操作問題而出現大的偏差。
隨着疫情進展,越來越多的檢測需求出現了。隨着居家隔離變成常態,自我檢測、自我採樣能不能可行?在美國第一個獲得藥監局批准的居家自助採樣試劑盒產品是LabCorp公司的產品Pixel,它用棉籤在鼻腔中抹一下,然後寄回到檢測中心做大規模檢測,這樣就不需要做很複雜的採樣。
目前,還沒有看到大規模的評價數據出現。但是畢竟拿棉籤捅鼻子,是不太容易做到很好的穩定性的,所以一個多月前,華西醫院的科研人員提出了用唾液進行新冠診斷的可能性。這是一個比較容易的自我採樣的操作。
近期,美國耶魯大學的科學家發表了一篇論文,比較了唾液和鼻咽拭子PCR核酸檢測的效果。實驗結果表明,和鼻咽拭子比,唾液採樣的穩定性相當不錯,甚至更好一些。另外更有意思的是絕大多數患者上看到的結果,唾液中檢測的病毒更多一些,結果可能更加準確,減少假陰性的出現。這是一個很好的起點,所以前幾天美國新澤西的Rutgers大學以及他們下屬的檢測機構獲得了美國藥監局的批准,開始使用唾液採集的樣品來進行新冠病毒的檢測。他們採用了一個流水線式的大規模處理的自動化機器,可以每天檢測1萬份樣本。唾液採樣檢測是非常令人鼓舞的新方法,如果得到推廣有望很好地解決我們過去採樣中的面臨的問題。
隨着疫情的第一個高峯過去,復工復學的階段到來,抗體檢測成爲新的流行語。抗體檢測是如何進行的?我發現前面九期都是跟這些問題相關的講座,大家肯定已經比我更加清楚什麼是抗體了。所以我就從技術上講講抗體檢測是怎麼做的。
首先樣本大不一樣,都是用血或者血清進行的檢測。抗體檢測的方法多種多樣,最常見的就是酶聯免疫吸附和免疫化學發光法。這兩個方法的原理非常像,也是實驗室研究最常見的檢測方式。以酶聯免疫吸附檢測原理爲例,在檢測基底上我們先鋪一層人工製備的抗原,然後把血清樣品加進去,孵育一段時間後,特異性結合到抗體上;然後我們把它洗脫,留下特異性結合的抗體;這時候加入酶標記的二抗,二抗能夠識別免疫抗體,它上面還帶催化作用的酶;然後再孵育一段時間,洗脫後留下特異性的二抗,加入一個底物會發生酶催化,從而導致顯色反應的發生,使得溶液的顏色深淺發生變化。最終我們用產生顯色反應的物質的濃度,推導出你想檢測的抗體的濃度。
這種方法,原理簡單,特異性通過抗體識別來保證,不需要特別複雜的操作,可以自動化或者半自動化,實驗通量不低。從這些孔中,顏色的深深淺淺,就可以算出抗體的多少。所以,這是一種定量的方法,也具備大規模篩查的能力。醫院裏使用的化學發光法和這個原理比較像,只不過檢測的信號不太一樣。
另外一個方法是利用膠體金顯色進行的試紙檢測方法,檢測是否懷孕的試紙用的也是類似的方法。這個方法的好處是非常簡單、易用、便宜,而且不需要複雜的設備,速度非常快。
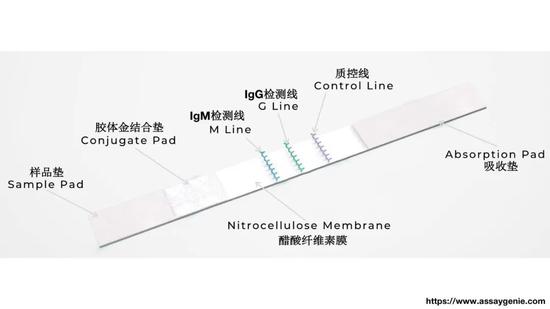
上圖是試紙條的結構:樣品墊、膠體金結合墊、醋酸纖維素膜和吸收墊。如果要檢測的樣品包括你想檢測的抗體,比如新冠病毒的抗體IgM或者IgG,將樣品送入試紙,這時候在膠體金結合墊上有金標抗原、金標單抗,即膠體金聯合的抗原和單抗,一起向質控線方向流動,金標單抗會結合到金標單抗的抗體上,作爲質控的結果。如果這個樣品裏面有這兩個待測抗體,它就會加到這兩個檢測線上,同時由於它能夠吸附金標抗原,所以會顯色。如果顯色了,就知道是否樣品中存在待測抗體。如果IgG這條線很深,就知道有IgG;而IgM這條線顯色非常淺,可以認爲也許沒有這個抗體,這個結果能夠很簡單地看懂。
爲什麼要做膠體金顯色檢測,是因爲這個實驗可以應用於大規模篩查。很多地方要調查感染率,如果感染率高,多數人有抗體,那這個病毒就不容易傳播。如果感染率很低,大多數人沒有抗體,病毒就很容易傳播,這是爲了更好地預防下一次的流行。
那麼做了檢測就能得到想知道的結果嗎?這需要非常認真地思考,因爲沒有一個方法是完美的。分子檢測從來都不是完美的,這世界上沒有完美的檢測方法。要了解每一種檢測方法的優勢和缺點,以便更好地選擇和判斷。
首先,檢測的時間點非常重要。

上圖是前幾天《美國醫學會志》上刊登的一個示意圖。不同的檢測對象和疾病進展間的關係有很大不同。病毒在發病前幾天才容易分離出來,那時候核酸載量是不多的。核酸檢測能檢測到嗎?咽拭子或者肺泡的灌洗液要比糞便檢測容易一些,但是糞便可能存在的時間長一些,後期更容易檢測出來。抗體都是在發病後期纔出來的,IgM抗體衰退比較快,IgG抗體衰退的慢,停留的時間會長一些。
所以選擇什麼樣的檢測方法,跟時間節點有極其重要的關聯性,每一個方法有極限。我們在分析中經常用檢出限來表示檢測方法的靈敏度,檢出限就是在給定的置信度條件下可以從被測樣品中檢測待測組分的最小濃度或者最小量。比如基因編輯方法檢測技術跟傳統的計算方法比,檢出限比傳統的RT-PCR方法高一個量級左右。實際上現在大量使用的RT-PCR的檢測限非常低,也就是說檢測的敏感性非常高,大概在一個反應能夠檢測幾個核酸片斷的存在。絕大多數其它檢測方法,快的也好、慢的也好,不見得敏感性更好。
另外,要考慮一個檢測方法的特異性是否真的很好。核酸檢測中特異性取決於引物選擇的位置、引物序列與目標核酸的匹配,還要考察是否真的能檢測出來。來自香港科學家的這篇發表在《臨牀化學》的研究論文表明,兩個核酸檢測位點總,有一個位點明顯比另一個更加容易檢測出來,具體說就是N蛋白基因比ORF1b更容易檢測出來,雖然一開始設計上看好像這兩個位點的表現都差不多,但是真正使用的時候是有區別的。
雖然方法都不是完美的,但是它也有一定的可取之處,只要用的妥當,找到號的適用場景。舉個例子,比如在人羣中35個健康人、35個感染者,我現在做一個檢測,檢測的陽性結果35個,大家認爲這是很不錯的結果,是吧?但事實卻不是這樣。檢測到的35個病人並不是真正的感染者。結果可以分成四塊:真實感染者檢測出來了,是真陽性;健康人被算成感染者,是假陽性;健康的人檢測出來健康,是真陰性;感染者未被檢測出來,是假陰性。所以真陽性、假陽性、真陰性、假陰性加在一起構成了整個檢測樣本的總數。
怎麼評價?第一個評價指標:敏感性。所有的陽性樣本中到底檢測出幾個陽性?分子是真陽性,分母是真陽性和假陰性的和。結果25個真陽性,10個假陰性,所以是71%的敏感度。
另一個指標:特異性,也就是陰性的樣本中有多少個真陰性。真陰性和假陽性一起當分母,而分子是真陰性。結果是25個真陰性,10個假陽性,一除還是71.4%。準確度,就是真陽性和真陰性的個數加起來除以總數,這樣算也是71.4%。很多場合我們都關心陽性結果是否真的是陽性?這就是所謂的陽性預測值(PPV),就是說當你看到檢測結果,真陽性和假陽性都是陽性,但是其中多少個是真陽性呢?這個例子中,25個真陽性,10個假陽性,PPV也是71.4%。也就是說測10個人大概有7個真陽性的,另外3個是假陽性。
剛纔我舉了一個非常奇怪的例子,可以看到很多數值算出來都是相同的,一個原因是由於例子中假陽性和假陰性測出來是一樣的。真實的檢測方法中間,不會特異性和敏感度都一定是一樣的。比如有這樣一個方法,也是同樣人羣檢測,我們發現所有的陰性樣本測出來都是陰性,但是陽性樣本中有5個測出來陰性。這時候發現它的特異性是100%,也就是說沒有假陽性。它的敏感性是86%,準確度是93%,PPV陽性預測值是100%。雖然這個檢測有假陰性存在,但是它沒有假陽性存在,所以測到的陽性一定是陽性,陽性預測值是100%。有沒有什麼樣的方法和它比較接近呢?是有的。比如我們用的PCR方法,如果做好了,它可以把陽性預測值做的很高。這是日內瓦的一個非盈利組織FIND,對市面上的部分試劑盒做了一個客觀評價,可以看到不同地方產的試劑盒,檢測不同的基因位點,雖然檢出限有高有低,但總的來說做的都非常好,特異性這個指標都非常高,很多都是100%。有這樣的方法存在,你就知道拿到檢測結果時,至少陽性預測值還是比較接近100%的。
剛纔舉的例子都是陽性和陰性樣本各佔一半的例子。這個例子在現階段新冠病毒疾病的情況下有點極端,不太適用。爲什麼?因爲陽性預測值跟傳染性疾病的感染率有關。舉個例子,500人的羣體裏做檢測,如果檢測方法的敏感性是95%,特異性是95%,而這個羣體感染率5%,結果是什麼樣呢?真實的感染者應該有25個,未感染者475人。但是檢測出來的結果是陰性452個,其中有1個假陰性,這個結果還好,說明如果你測出來的結果是陰性的,你是真的陰性的概率是99.8%,這還是相當不錯的。
但是,測陽性的結果不容樂觀。本來只有25個陽性樣品,愣是測出來了48個陽性結果,其中24個真的,24個假的。所以真陽性的概率50%,也就是說,你的結果是陽性的話,也有一半的可能你體內並沒有抗體,你可不能出去瞎逛,還是老老實實待在家裏比較好。
剛纔說的是感染率5%的情況,如果感染率達到25%,又會是什麼結果?大概500個人裏面應該有125個感染者,測的結果裏有6個假陰性、19個假陽性。如果結果是陰性結果,大概98.3%的概率是真陰性,也還不錯。如果是陽性結果,真陽性概率86%,說明你還是有不小的可能,體內沒有抗體,你還要出去瞎逛嗎?
剛纔舉的例子是基於抗體檢測的試劑表現挺好的一個假設,即假設試劑的檢測敏感性95%、特異性95%,而這並不是那麼好做的。
我們想象一下如果這倆指標沒有那麼高的情況吧。假設有一個大城市,感染率爲1%,我們坐一個1000人的抗體檢測。所用的檢測試劑敏感性90%、特異性80%,這個值符合現在不少試劑的真實指標。那會有什麼樣的結果呢?1000人裏面,因爲感染率是1%,所以真正有抗體的人應該有10個,沒有抗體的人有990個。這10個人裏面,由於檢測試劑的敏感性是90%,所以有9個檢測出來是真陽性,1個是假陰性。在沒有抗體的人裏面,因爲檢測的特異性是80%,所以其中990個人裏面有792個被測成真陰性,但是198個人出現了假陽性。
所以,檢測結果出來後是這樣的,測了1000人,結果207個呈現陽性,793個陰性。這說明一個人如果測到陽性結果,實際上只有4%的幾率是真陽性,有96%的可能性並不是陽性。怎麼改變這個狀態呢?根本的解決方法就是把試劑做的越來越好,比如說再增加一些特異性。假設特異性增加到90%,這個結果就變了,假陽性減少到99個人。
但是這個結果,陽性預測率只從4%提高到8%,陽性結果中還是有90%以上的假陽性。假設特異性增加到99%,陽性預測率可以增長到47%左右。99%的特異性對抗體檢測來說是很大的難題,因爲這已經是非常高的指標了。這也是爲什麼檢測能力不夠理想的抗體檢測在感染率低的情況下做大規模篩查是有很大問題和風險的,我們一定要把統計學的基本概念牢牢記在心裏。
前幾天美國加州的一幫科學家聯合在一起組織了互助合作社,他們橫向比較了不同的抗體檢測方法,共進行了12種方法,10種是試紙條,2種是酶吸附。試紙條裏面很多是中國廠商的產品,也有美國廠家的產品,結果看上去都差不多,並沒有哪個特別一枝獨秀。所以並不是說大家生產能力差別很大,而是這個方法的挑戰本身是普遍性的。

上圖可以看到敏感性,在早期的時候不是特別好,很可能是由於檢測的時候抗體本身濃度低,所以檢出率低。慢慢敏感性增加,後期大概80%或90%。特異性差別很大,有的相當好,有的其中某個指標很不錯,有的綜合考慮起來的也還可以。大部分廠家在80%、90%左右,小樣本比較裏,有的方法達到100%。所以抗體測試,尤其是膠體金測試中,總體上看,假陽性率是一個大問題。
如何做特異性測試呢,是利用新冠核酸陰性的樣品。因爲沒有辦法從現在大規模流行進行的時候的樣本中,找到真正的肯定的陰性樣本來做質控,只好採用新冠肺炎之前,2018年7月份之前的樣本測試交叉檢驗,最後看出來它到底會不會有陽性的出現。他們做了很嚴格的比較,結果很有意思。
可以發現這些方法都相當不錯,他們的方法穩定性都相對不錯,只不過現在爲止沒有哪個方法真的具備和核酸檢測一樣穩定和優秀的特異性,不能完全相信它的結果,所以假陽性問題一直會困擾我們。
超越核酸檢測:測序檢測法
最後花點時間講講是否有超越核酸檢測的其它檢測方法,比如測序。測序是過去幾年才被大家提上日程的檢測方法。
過去幾個月,我們正好有一個方法基本成型了,1月份的時候我、清華的王建斌和我們中心謝曉亮教授一起發表了一篇論文。這個論文中報道了一個新的簡便的RNA測序的處理方法,取名SHERRY。把樣品放進去之後,用三步法就形成了測序,大大降低了以前這些對實驗技巧要求非常高的實驗操作的難度,可以使實驗結果更加穩定、可靠和快捷獲取。在新冠病毒肆虐的時候,醫院都在超負荷運行,醫院的科研人員也沒有太多時間去想複雜的操作流程,所以越簡單的操作流程越有利於爲臨牀新冠測序服務。
過去幾個月,我們雖然不能全面復工,但是我們有幸和北京地壇醫院的合作者一起,在SHERRY基礎上開發了新方法,叫MINERVA,這個方法的出發點就是真從實際出發考慮,如何爲臨牀服務。這個方法不怎麼挑樣本,咽拭子、痰、糞便都可以,經過提取之後建立第一步的SHERRY文庫,再經過富集等步驟就會有一個新的文庫做病毒全基因組測序。
通過這個測序我們研究了80多個樣本的核酸序列,從中可以看到之前很多沒有辦法用簡單的核酸PCR檢測手段獲取的信息。我們看到了很有趣的現象,比如很多樣本在特定位點中都可能有不同的突變。這是一個全新的病毒,對這個病毒瞭解得越深刻,越有利於我們防控疫情,也爲未來可能的威脅做好準備。
另外,我們並不知道這個病毒的突變是如何發生的。突變和疾病發展有什麼關係?以後會不會影響到分子檢測試劑的研究?它的準確度還能不能保證?突變是不是影響疫苗開發?是不是影響藥物實驗?這些我們都不知道,所以需要有更多工具來研究。
最後我要感謝北京大學的謝曉亮教授的指導,很多檢測實驗的細節請教了中國醫學科學院的任麗麗研究員以及一線工作的中國醫學科學院的吳晨教授,還有長期合作者清華大學王建斌教授。通過這次疫情,我們跟地壇醫院的陳晨研究員團隊同心協力獲取了大量的基因組數據,爲未來的研究打下了基礎。還有感謝在疫情期間堅持工作的學生和工作人員,他們付出了巨大的努力使得我們能夠完成這個結果。我的工作主要是在北京市教委支持的北京未來基因診斷高精尖創新中心和北京大學生物醫學前沿創新中心完成的,這兩個中心都是謝曉亮教授領導的多學科交叉的研究基地。我們側重於微量核酸樣本的分析和測序研究,希望能夠在不遠的將來給大家帶來更多的結果。
(注:本文根據黃岩誼教授在《理解未來》科學講座:病毒與人類健康-專題科普”第十期演講整理而來,有刪減,PPT圖片由講者提供,未經允許不得使用)
推薦
《科學大家》專欄投稿郵箱:[email protected] 來稿請註明姓名、單位、職務