边造变种病毒边卖疫苗,称疫苗生意“摇钱树”?辉瑞否认
编辑 | 西尔维亚
一觉醒来,#辉瑞# 和#辉瑞考虑自行研发COVID病毒变种# 一道挂在热搜上。
被质疑自研COVID病毒变种,辉瑞最新回应
据大河报报道,近日“真相工程”爆出卧底暗访辉瑞主管的谈话视频,视频中提到,辉瑞考虑自行研发COVID病毒变种,疫苗生意是“摇钱树”,监管人员睁一眼闭一眼等内容。


有网友直言,这就像“杀毒软件自己研发病毒自己杀一样”。2010年左右,瑞星杀毒造假案曾轰动一时,第一财经援引国内某知名PC厂家高层消息称,“这其实是杀毒软件行业里的公开秘密”。制造病毒和查杀病毒有点像间谍和反间谍游戏,如果没有病毒,查杀病毒也无从谈起。只有病毒越多越厉害,杀毒软件才能更畅销。
不过,这则热传视频的真实性、客观性有待考究,所谓“辉瑞主管”的身份也有待确认。
1月27日,辉瑞在官网发文回应,最近有人指控辉瑞公司的功能增益和定向进化研究,该公司希望澄清事实。
辉瑞表示,该公司在COVID-19疫苗的持续开发中,未进行功能获得或定向进化研究。但辉瑞与研究者合作,原始SARS-CoV-2病毒已被用于表达值得关注的新变种刺突蛋白。该研究提供了一种快速评估现有疫苗诱导抗体的能力的方法,以此用作确定是否需要更新疫苗的步骤之一。
辉瑞在声明中提到,在有限的情况下,当完整的病毒不包含任何已知的功能突变增益时,可以设计这种病毒以评估细胞中的抗病毒活性。其强调,它们的研究是美国和全球监管机构要求对所有抗病毒产品进行的,并由美国和世界各地的许多公司和学术机构进行。植根于合理科学的事实信息对克服COVID-19大流行病至关重要,辉瑞公司仍然致力于提高透明度,帮助减轻这种疾病的破坏性负担。
新冠之后,辉瑞的社会责任和经济收益
至今已有170余年历史的辉瑞,从青霉素发家,又靠伟哥暴富,是目前全球处方药销售规模最大的药企。疫情爆发后,辉瑞研发的新冠疫苗Comirnaty和新冠口服药Paxlovid引发外界热议和全球关注。2020年底,Comirnaty于美国获批并开打;2021年底,Paxlovid的紧急使用授权申请在美国被批准。
据虎嗅报道,Paxlovid上市之前,辉瑞就与非营利机构“药物专利池”(简称MPP)达成许可协议。而通常制药企业会等到新药获得足够盈利之后,才考虑“行使社会责任”,将专利授权给MPP。
根据协议,“药物专利池”可向95个国家的合格仿制药企授权生产Paxlovid的仿制药,并免除授权使用费。这95个国家和地区,包括所有低收入和中低收入国家,以及部分中高收入国家,大约覆盖全球约53%的人口。或许正如辉瑞ESG报告中提及:“从一开始,辉瑞应对新冠疫情的策略,就没有把它当作平常生意来做。”
不过,这两款应对新冠的明星产品的确给辉瑞带来巨大收益。
2022年11月,辉瑞披露三季报,22年Q3新冠疫苗Comirnaty直接销售和相关收入达到44.02亿美元,较去年同期下降66%。新冠口服药Paxlovid口服药物Paxlovid持续增长强势,全球销售额达到75.14亿美元。从辉瑞目前的营收结构来看,Comirnaty和Paxlovid在Q3收入中分别占到19.4%和33.2%,新冠产品在其营收中占比已经超过一半。
今年前三季度,辉瑞靠新冠疫苗整体收入264.77亿美元,同比上涨9%,新冠口服药收入171.99亿美元。值得一提的是,三季报中辉瑞上调了新冠疫苗Comirnaty的2022年营收指引,从320亿美元上升至340亿美元。新冠口服药Paxlovid的营收指引仍为220亿美元。
据第一财经援引英国商业数据公司GlobalData观点,Paxlovid的前10年销售总收入将达到800亿美元,其中仅是2022年的销售就占据很大一部分。并且GlobalData预估,自2023年起,Paxlovid的销量会逐年递减,呈现明显的下滑趋势。而这一趋势的原因来自于新冠病毒毒性的持续下降以及疫苗加强针的推广。
据澎湃新闻援引《华尔街日报》1月18日报道,辉瑞公司CEO艾伯乐在世界经济论坛期间表示,新冠病毒可能会一直存在,辉瑞正努力开发效果能够持续一年的新冠疫苗。
艾伯乐认为,新冠疫情已持续三年,但某种程度上,世界并未对下一次全球健康危机做好准备。他表示,对于如何应对疫情,各国政府尚未做出改变,且某些情况下还采取可能妨碍药物开发和创新的监管措施。对于世卫组织和美国疾病控制与预防中心,艾伯乐表示不满。他提出,“新冠带来的重大教训是什么?是幸好有一个既有私人推动但也有学术界支持的蓬勃发展的生命科学产业。”
医保谈判失败,辉瑞将推动paxlovid在中生产
2022年2月,Paxlovid在中国附条件紧急获批,成为中国首个获批的口服小分子新冠药物。同年3月,Paxlovid被纳入《新型冠状病毒肺炎诊疗方案(试行第九版)》,其适应症为发病5天以内的轻型和普通型、且伴有进展为重症高风险因素的成人。
1月8日,中国国家医疗保障局发布消息,辉瑞新冠口服药Paxlovid因企业报价高未能通过谈判纳入医保目录。不过按现行的新冠药品报销政策,Paxlovid仍可临时报销至2023年3月31日。
1月9日,辉瑞公司CEO艾伯乐在JP摩根医疗健康大会上表示,正在与中国的合作伙伴合作,从今年上半年开始在中国提供新冠口服药Paxlovid。据其透露,该合作伙伴的生产尚未开始,但很快会启动,“即使在未来3~4个月内就实现这个目标,我也不会感到意外。”
据界面新闻报道,2022年8月,辉瑞的在华子公司辉瑞投资有限公司曾与华海药业签署生产与供应协议,由华海药业在协议期内为辉瑞在中国大陆市场销售的Paxlovid提供制剂委托生产服务。其中,辉瑞提供奈玛特韦原料药与利托那韦制剂,华海药业负责奈玛特韦制剂生产,并完成组合包装。
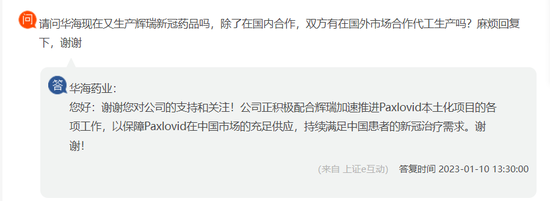
1月10日,华海药业在上交所互动平台回应称,目前公司在加速推进辉瑞产品本地化生产项目的各项工作,以保障Paxlovid在中国市场的充足供应。但目前Paxlovid本土化还没有批下来,业内人士认为,若辉瑞的合作伙伴,如华海药业的工艺验证、清洁验证等都没有问题,也有空置的生产线专门用来生产相关产品,预计从申报到上市的时间大约在三到四个月。
这样算起来,临时医保到期之际,Paxlovid或许将迎来其中国本土化生产。而值得注意的是,去年12月底,默沙东新冠口服药莫诺拉韦在国内应急获批,成为继辉瑞的Paxlovid、河南真实生物的阿兹夫定之后,国内第三款获批的新冠口服药。市场竞争加剧,Paxlovid届时的本土生产和市场表现仍然充满未知。









