過量果糖會引起腸道屏障受損,炎症增加,促進肝臟中脂肪沉積變性
來源: 奇點網
大家知道在所有天然糖中,甜度最高的是哪種嗎?答案是果糖。果糖一度是被大肆表揚的“健康糖”,因爲更甜的同時升糖指數卻比其他天然糖低。
但果糖真有那麼健康嗎?未必。因爲它可能是非酒精性脂肪性肝炎(NASH)的推動者。在人羣研究中,果糖攝入與肝臟脂肪增加、炎症和纖維化的發展有關,它在導致肝臟脂肪積累方面的能力是葡萄糖的數倍,而NASH是肝癌的一大重要原因。
但研究人員們之前一直不知道果糖是如何做到這一點的,在最近的《自然·代謝》雜誌上,美國加州大學聖地亞哥分校的研究人員發現了其中的機制。
原來,大量果糖進入腸道後,被果糖激酶分解,會引起內質網應激和腸道炎症,導致腸道屏障受損,細菌逃逸,進而發生內毒素血癥,增加的促炎細胞因子會誘導肝臟中的脂質合成、囤積和變性,從而促進了NASH的發生。

圖片來自pixabay.com
在這項研究中,研究人員先使用高果糖飲食(60%能量來自於果糖,10%來自於玉米澱粉,易水解爲葡萄糖)餵養基因工程改造過的NASH模型小鼠,對照組則採用總能量相同的玉米澱粉飲食,70%的能量來自於玉米澱粉。
兩組小鼠的攝入量差不多,高果糖組很快表現出了明顯的肝臟脂肪變性和甘油三酯水平的增加,而玉米澱粉組則沒有。6個月時,高果糖組小鼠出現了胰島素抵抗、脂肪性肝炎和肝纖維化。12個月後,高果糖組小鼠的肝臟腫瘤比玉米澱粉組大3倍,腫瘤負荷高10倍。
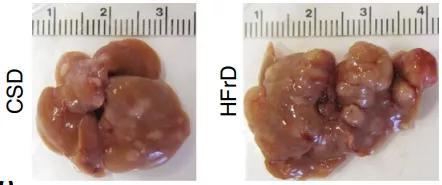
玉米澱粉組(CSD)和高果糖組(HFrD)小鼠肝臟腫瘤對比
另外,小鼠的結腸變短,說明有腸道粘膜炎症。不但如此,長期的高果糖飲食餵養還導致了腸道屏障受損,這主要表現在小鼠腸道中緊密連接蛋白的mRMA水平降低,緊密連接蛋白減少,這個蛋白是細胞間連接的紐帶,和腸上皮細胞共同組成腸道屏障。
腸道粘膜炎症是導致緊密連接蛋白減少的一個原因,而又是什麼導致了腸道粘膜炎症呢?他們發現,類似於遺傳因素導致的果糖不耐受,果糖代謝產物果糖-1-磷酸干擾了N-糖基化,而N-糖基化缺陷觸發了內質網應激,小鼠幾個與內質網應激有關的標誌物水平都有明顯上升,這才導致了腸道粘膜炎症,也損害了緊密連接蛋白的組裝。
腸道屏障受損後,小鼠的腸道微生物從腸道中逃逸,血液檢測表明小鼠出現了內毒素血癥,用抗生素治療可以幾乎完全抑制內毒素血癥,還阻止了肝臟脂肪變性,減少了肝臟腫瘤的發生。
通過對比高果糖組小鼠和玉米澱粉組小鼠在不同階段的肝臟和炎症相關轉錄組,研究人員發現,在9個月大的小鼠中,肝癌相關特異性基因表達水平升高,非腫瘤相關的,與傷口癒合、細胞粘附和先天免疫等基因的表達也發生了巨大變化。

圖片來自pixabay.com
進一步研究發現,高果糖組小鼠肝臟中,與先天免疫有關的Toll樣受體2和Toll樣受體4等磷酸化水平增加,抗生素治療時,這種變化也會消失。它們的表達增加最可能發生在肝臟招募的巨噬細胞中。
激活的巨噬細胞是促炎因子,腫瘤壞死因子(TNF)的主要來源,人的原代肝細胞體外培養試驗表明,在用內毒素(脂多糖)和TNF處理的情況下,與果糖共同培養的肝細胞纔會明顯出現更強的脂質液滴的積累,而如果只有脂多糖,沒有TNF,也是無法達成這一點的。
也就是說,果糖導致的腸道屏障受損和內毒素血癥是通過巨噬細胞分泌的促炎因子TNF來介導肝臟脂質積累的。
給小鼠補充整合蛋白介導的IL-6,可以通過基質蛋白CCN1促進緊密連接蛋白的修復,或者活化腸上皮gp130信號,通過STAT和YAP通路,促進修復。腸道屏障的完整性得到保障,也就抑制了高果糖飲食導致的細菌逃逸和內毒素血癥。
這些小鼠成功抵抗了果糖誘導的肝臟中腫瘤的發生,而且肝臟中與炎症和脂質合成有關的基因的mRNA表達也沒有出現明顯增加。

圖片來自pixabay.com
研究人員表示,在美國,有1/3的人受到非酒精性脂肪性肝病的困擾,雖然每天攝入一定量的果糖不會造成明顯危害,只有長期超量攝入纔會,但現實是,很多加工食品中都含有果糖,大多數人無法很好地估算他們實際上攝入了多少果糖。
他們認爲,現在需要一方面提高大家對果糖過量攝入的危害的認識,另一方面,對於已經發展爲脂肪性肝病的患者來說,或許基於腸道屏障修復的治療方法會是新的潛在治療手段。