面對阿爾茨海默病,爲何女性更危險?
摘要:莫斯科尼的PET結果證明,更年期(通常在45~55歲之間)女性體內雌激素水平的下降,會導致她們的大腦出現“生物能量危機”。”她說,每個人,尤其是處於四五十歲的女性,都應該“知道自己患病的風險”,包括ApoE基因狀態、代謝特徵、血液生化指標甚至是大腦掃描圖譜,尤其是在性別特異性的圖像標記物出現時。
撰文 | 傑納·平科特(Jena Pincott)
翻譯 | 劉宏麗
索菲(Sophie,化名)告訴我她的記憶力是如何開始衰退的:她出現在辦公室準備工作,卻忘記了自己原本和客戶有一個早餐會;大腦裏一片空白,完全想不起鄰居們的名字;她進入一個房間,卻絲毫記不起自己爲什麼會在那裏。索菲是一名50歲出頭的律師,她已經進入更年期,經常會出現潮熱和夜間盜汗等現象。但索菲的健忘似乎與這些現象無關,那她的大腦到底怎麼了?
莉薩·莫斯科尼(Lisa Mosconi)是韋爾康奈爾婦女大腦倡議組織(Weill Cornell Women‘s Brain Initiative)的主任以及威爾康奈爾醫學院阿爾茨海默病預防中心副主任,她可能知道這是怎麼回事。她已經分析了數千例進入更年期的女性患者的正電子發射斷層掃描(positron-emission tomography,PET)圖像,並且觀察了她們大腦的新陳代謝速率隨時間的變化。莫斯科尼說:“在絕經前,女性大腦的能量很高。”她向我展示了一張年輕女性大腦的PET圖像,上面有許多反映高水平葡萄糖代謝的亮紅色和橙色斑點,顯示出大腦的神經元活動。
當女性處於圍絕經期(更年期之前的一段過渡時期)時,她們大腦中的葡萄糖代謝速率會減慢10%~15%或更多,掃描結果也發生了變化:亮紅色和橙色斑點會更多地被黃色和綠色斑點取代,這表明大腦攝取的糖分減少,新陳代謝速率降低。莫斯科尼說:“絕經後,女性大腦中的葡萄糖代謝速率會下降20%~30%,有時會更多。”
在年輕女性的大腦中,雌激素是主要的新陳代謝調節因子,負責從葡萄糖轉運、攝取到分解產能的全部代謝過程。莫斯科尼的PET結果證明,更年期(通常在45~55歲之間)女性體內雌激素水平的下降,會導致她們的大腦出現“生物能量危機”。在這段超過7年的過渡時期,高達60%的女性會出現更年期相關的認知障礙,包括一陣陣的記憶力混亂、注意力分散和健忘。神經突觸的形成需要能量,但隨着大腦中雌激素水平和葡萄糖代謝能力的降低,神經元之間新的神經突觸的形成速度會隨之下降。幸運的是,這種損傷只是暫時的。隨着大腦產生補償機制,並利用其他來源的能量,她們的情況會好轉,認知能力也能恢復。
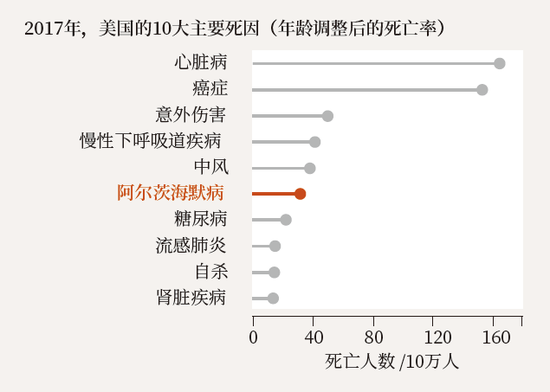
在美國,阿爾茨海默病是第6大死因。專家指出,由於死亡原因通常根據直接死因判斷,如患者死於肺炎而不是潛在的癡呆症,因此阿爾茨海默病導致的死亡率可能被低估了。
2009年的一項研究指出,剛絕經的女性的認知測試得分和過渡階段之前一樣好,但在數十年後,其中約1/5的人被診斷爲阿爾茨海默病。莫斯科尼等人認爲,在美國的360萬阿爾茨海默病女性患者中,更年期可能是認知能力下降的一個臨界點。
但在涉及女性特有的患病風險因素、症狀、預防和對治療的反應時,仍有太多問題沒有答案。爲什麼在美國當女性到達65歲時,就有1/5的可能性患上這種疾病,而同年齡的男性比例卻只爲1/9?
更年期假說認爲女性在更年期時雌激素水平下降,會使大腦在將來面對損害時更加脆弱,這或許可以爲上述問題給出答案。如果莫斯科尼等人是對的,包括索菲在內,經歷這一過渡時期的女性將能受益於生活方式干預,以及存在爭議但具有預防效果的激素療法。
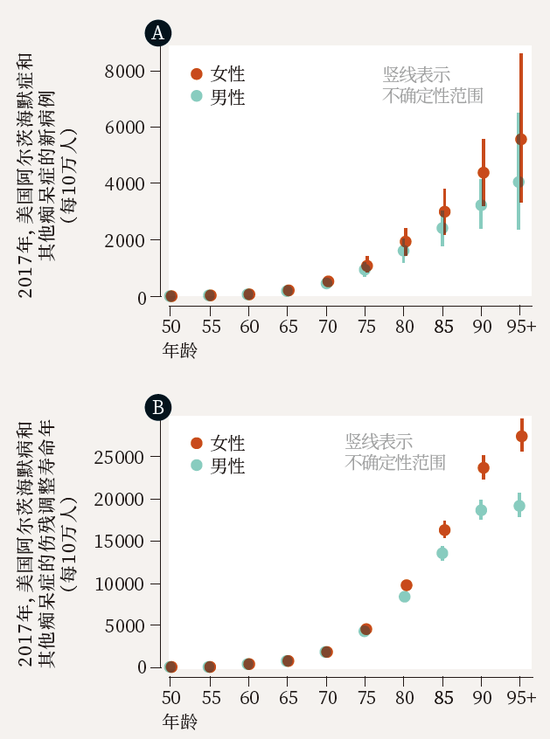
根據華盛頓大學健康指標與評估研究所(IHME)的估計,美國女性患阿爾茨海默病的比例高於男性。從50歲開始一直到95歲,在新診斷的病例中,女性患者越來越多。用疾病導致喪失生活能力或早死的年數(基於平均壽命)來衡量疾病時,女性和男性之間的差異同樣在逐漸增加。
失去雌激素
在描述絕經女性體內雌激素下降、PET圖中主要爲綠色斑塊時,亞利桑那大學腦科學創新中心主任羅伯塔·迪亞斯·布林頓(Roberta Diaz Brinton)表示:“大腦進入了飢餓模式。”她解釋說,在大腦生物供能中,雌激素擁有廣泛的功能。作爲一種信號分子,雌激素在整個大腦中到處都有受體,它可以調節線粒體爲神經元和神經元間連接的形成提供能量。雌激素能激活促使神經突觸發揮功能的酶,還能促進葡萄糖從血管轉運到大腦、從大腦運輸到神經元,以及支持和保護神經元的神經膠質細胞。
布林頓對老年雌性小鼠的研究顯示,隨着雌激素水平下降和葡萄糖代謝速率減慢,大腦會使用酮體供能。酮體是由脂肪酸產生的物質,在這種情況下,酮體來自白質(包括保護神經元的髓鞘)。而這種轉變在本質上是一種自我蠶食行爲,在一定程度上會出現在女性體內。那些更多地依賴酮體爲大腦供能的人,可能會面臨更嚴重的白質退化和更高的癡呆風險。
莫斯科尼說,相比於四五十歲女性的大腦,同年齡段男性的大腦並沒有出現明顯的老化,出現β-澱粉樣蛋白斑塊的比例也更低。一種解釋是,睾酮和雌激素一樣,具有保護神經的作用。男性在該年齡段時,體內的睾酮水平不會像女性的雌激素一樣急劇下降。這種差異可能有助於解釋,爲什麼男性患阿爾茨海默病的概率較低。
爲了進一步明確患病風險較高的女性,研究人員已經開始研究阿爾茨海默病與暴露在雌激素環境的時間的聯繫。科學家用“生育期”(女性第一次月經和最後一次月經之間的時間跨度)來衡量雌激素的暴露時間。一項對凱撒醫療集團(Kaiser Permanente)醫療保健聯盟的15 754名女性成員的大規模研究發現,生育期爲21~34年的女性患癡呆症的概率比生育期爲39~44年的女性高26%。這一結果表明,月經期開始較晚或結束較早的女性患阿爾茨海默病的風險更高。
然而,還有很多因素能影響女性的雌激素暴露時間,但它們對阿爾茨海默病的影響並沒有得到充分的研究。一些研究試圖將女性生育次數與阿爾茨海默病的患病風險聯繫起來,但得到的是矛盾的結果。全世界有超過1億女性服用避孕藥來抑制卵巢激素的分泌,然而令人震驚的是,對於避孕藥對癡呆症風險的長期影響,我們還知之甚少。

激素療法
索菲在青春期時就開始服用避孕藥,她從未生育過。她表示,在圍絕經期的最後一年,她的記憶力衰退達到了頂峯。她經常會在一小時內經歷3次以上的潮熱,這一頻率和嚴重程度與加劇白質損失、增加大腦中葡萄糖代謝失調和晚年患癡呆症的潛在風險有關。索菲的醫生給她開了一種新的藥物:雌激素-孕激素複方片(孕激素可以保護子宮)。索菲說,這個藥物的效果“不可思議”:她的潮熱消失了,而且重新想起了早餐會議。
爲了大腦的健康,每個更年期女性都應該接受激素治療嗎?實際情況要更加複雜。21世紀初,美國國家心肺血液研究所報告了來自女性健康倡議研究和輔助記憶研究的結果。結果顯示,激素療法(包含雌激素和孕激素)與乳腺癌、中風、心臟病和血栓的風險增加有關,令人驚訝的是,激素療法使用者的癡呆症發病率高出一倍。
女性服用第一粒激素藥丸(或是使用乳膏或貼片)的年齡,正好是布林頓所說的“雌激素偏向於在健康細胞中發揮作用”的時間。如果神經元是健康的,它們會對雌激素產生反應。但如果神經元老化或缺乏雌激素刺激的時間過長,會導致相關的信號通路退化以及受體功能失調,進而喪失對雌激素的反應。在這種情況下,補充雌激素甚至會加劇神經退化。布林頓說,要讓激素療法產生有益而非有害的作用,女性必須在關鍵窗口期內開始服藥,通常是停經後的5年內。
一些觀察性研究通過測試使用激素療法至少10年的患者,檢驗了關鍵窗口期假說。其中,一項在猶他州開展的研究指出,在更年期開始的5年內,使用這種療法能使阿爾茨海默病的患病風險降低30%;而在芬蘭的一項近期研究中,該療法卻使患病風險增加了9%~17%,且開始使用的年齡並不會影響患病風險。我們應該相信哪個結果?研究人員也不清楚。莫斯科尼說:“我們還需要更多的臨牀試驗,尤其是針對那些從圍絕經期就開始激素治療的女性。”
脆弱的更年期
在最開始,更年期與阿爾茨海默病的聯繫並不明顯。女性絕經的平均年齡爲51歲,而診斷出阿爾茨海默病的平均年齡爲70~75歲,兩者之間存在20多年的差距。但是,這一疾病的前驅階段(從出現β-澱粉樣蛋白等病理特徵到全面認知障礙),大約也會持續20年。“這也許只是時間上的巧合,”布林頓說,“但我不這麼認爲。”
在腦部掃描之外,有沒有可能在女性還健康時,就更早地預測出她們患阿爾茨海默病的風險?在一項發表於2016年的研究中,布林頓等人將500名健康的絕經後女性分爲3組,分別是代謝最佳組、高血壓臨界組和代謝健康臨界組。在語言記憶測試中,只有代謝健康臨界組的得分明顯更低。
嚴格來說,這些受試者的代謝指標仍在正常範圍內,但有跡象表明她們的身體狀況正朝着不健康的方向發展。例如,在這一組中,30%的女性血糖水平接近患前驅糖尿病的閾值,而這種情況與認知障礙有關。對許多處於過渡階段的女性來說,前驅糖尿病是患II型糖尿病的開端,而後者幾乎使患阿爾茨海默病的風險增加一倍。超過80%的阿爾茨海默病患者出現了胰島素抵抗。
一旦認爲更年期會改變女性全身的生理狀態,我們很容易看到一系列複雜的因素如何引發阿爾茨海默病,以及爲什麼控制這些因素是預防的關鍵。雌激素對心血管系統的健康效益包括膽固醇調節,它可以提高“好的”高密度脂蛋白(HDL)膽固醇水平,並降低“壞的”低密度脂蛋白(LDL)膽固醇水平,後者會導致脂肪和蠟樣沉積物在動脈中堆積。ApoE基因能介導膽固醇的新陳代謝並將其輸送到神經元,但ApoE4變體攜帶者的血液中LDL膽固醇水平較高,常常伴隨動脈硬化。當他們體內的炎症反應使這些沉積物散開時,還可能導致“無症狀性中風”,這又將會使患阿爾茨海默病和其他類型的癡呆症的風險增加一倍以上。
睡眠在大腦的新陳代謝的調節(如增強對胰島素的敏感性)中也起到關鍵作用。睡眠不足對女性,尤其是處於更年期女性的影響更加嚴重。在正常休息的夜晚,神經膠質細胞會將大腦中的β-澱粉樣蛋白和tau蛋白排出。但睡眠不足會破壞這個過程,這些蛋白質在大腦中堆積並形成斑塊。這會導致睡眠支離破碎,損害神經細胞的葡萄糖代謝,而這又會進一步干擾睡眠。因此,大腦進入這個危險的循環後,會加速神經退化的進程。
壓力也能改變更年期中的臨界點。一項長達35年的追蹤研究發現,壓力持續超過一個月,或者女性在四五十歲時遭受更多的壓力,在40年後患阿爾茨海默病的可能性就越大。除了壓力,女性比男性更有可能患上抑鬱症,這幾乎會使癡呆症風險翻倍。
預防與新療法
2019年,布林頓等人發表了關於代謝標誌物研究的後續結果,並將ApoE基因的狀態作爲一個新變量。攜帶ApoE4基因單拷貝的人約佔美國總人口的25%,這些人更容易患上阿爾茨海默病,約佔所有病例的40%。女性攜帶者比男性攜帶者發病更早,通常在65~75歲之間,這可能是因爲喪失了雌激素對神經的保護作用。
與布林頓之前的研究一樣,新陳代謝狀況不佳的一組在一些認知測試中得分較低。但這次的分析揭示了,攜帶ApoE4基因是這一組表現不佳的主要原因。在這些攜帶者體內,高膽固醇和由不良代謝帶來的其他健康影響,會加劇ApoE4的負面影響,導致早期認知能力的下降。然而,對這些攜帶者採用激素治療干預後,他們的代謝狀況會得到改善,同時在某些認知測驗中的得分也會提高。
但布林頓認爲攜帶ApoE4基因只是“敲響了警鐘”,而不是“宣判死刑”:許多攜帶ApoE4基因的女性並沒有患上阿爾茨海默病。在她的研究中,最佳代謝健康組在認知測試中得分最高,這其中就包括該基因的攜帶者。
根據2017年《柳葉刀》雜誌的一篇報告,至少三分之一的阿爾茨海默病病例與糖尿病、肥胖、不良飲食和其他可預防或治療的因素有關。布林頓總結說:“關鍵的信息是維持新陳代謝健康,可以維持認知健康”。莫斯科尼對這一觀點表示贊同,“我們無法改變染色體性別、年齡或攜帶的基因變體,但可以改變代謝的健康狀況,從而降低患病風險。”她說,每個人,尤其是處於四五十歲的女性,都應該“知道自己患病的風險”,包括ApoE基因狀態、代謝特徵、血液生化指標甚至是大腦掃描圖譜,尤其是在性別特異性的圖像標記物出現時。
激素療法是否應該被納入治療方案,仍存在爭議。但布林頓說,包括基因測試和數據分析的精準醫療已經應用於激素療法,醫生可能很快就會根據一些風險生物標誌物,如ApoE基因狀態、生育史、更年期症狀等因素,給出精確的治療方案。而新形式的激素療法正在研發中。
還有一些阿爾茨海默病病例是無法預防的,對此,布林頓實驗室正在開發一款以異戊烷醇爲原料,名爲Allo的藥物。異戊烷醇是一種天然存在的類固醇,它可以刺激新的神經元形成。在阿爾茨海默病小鼠模型中,Allo逆轉了小鼠認知缺陷,使它們恢復了學習和記憶能力。布林頓說,該藥物治療ApoE4攜帶者的Ⅱ期臨牀試驗,計劃於今年晚些時間啓動。這一試驗由美國衰老研究所資助。
2016年,美國國立衛生研究院(NIH)開始要求其資助的研究將性別作爲一個生物學變量。由於阿爾茨海默病的病程發展緩慢,這也意味着,這些研究需要經過多年時間,才能使更年期過渡期的女性受益。
與此同時,預防仍然必不可少,特別是對於中年女性。建議包括:以植物爲主的低糖、低反式脂肪和低飽和脂肪飲食,體育鍛煉,減輕自身壓力,以及每晚7小時的睡眠(清理β-澱粉樣蛋白和tau蛋白)。布林頓說:“女性總是優先照顧別人,並把自己放在最後,但女性更需要重視自己的健康問題。”







